题目内容
13.下列叙述正确的是( )| A. | 有化合物生成的反应一定是化合反应 | |
| B. | 由同种元素组成的物质一定是单质 | |
| C. | 有发光放热现象的变化一定是化学变化 | |
| D. | 化合物中元素正负化合价的代数和一定为零 |
分析 A.根据化合反应的判断方法来分析;
B.根据单质的概念来分析;
C.有发光、放热现象发生的变化不一定是化学变化;
D.根据化合价的规定来分析.
解答 解:A.化合物反应是由多种物质反应生成一种新物质的反应,但是有化合物生成的反应不一定是化合反应,如在加热的条件下,氢气与氧化铜反应生成铜和水,生成物中的水是化合物,但该反应不属于化合反应,故错误;
B.由同种元素组成的物质不一定是单质,也可能是混合物,如氧气和臭氧的混合物是由氧元素组成的,故错误;
C.有发光、放热现象发生的变化不一定是化学变化,如通电时灯泡发光、放热,属于物理变化,故错误;
D.化合物中各元素正负化合价的代数和一定为零,故正确.
故选D.
点评 本题考查的知识点较多,掌握化合反应的概念、单质的概念、化学反应的现象以及化合价的原则是解题的关键.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
11.下列事实用微粒的知识解释正确的是( )
| 选项 | 事实 | 解释 |
| A | 食醋有酸味 | 醋酸分子有酸味 |
| B | 紫罗兰花瓣遇盐酸变红 | 溶液中存在不断运动的氯化氢分子 |
| C | 分离液态空气制氧气是物理变化 | 原子种类没有改变,原子间的间隔变大 |
| D | 一氧化碳有毒,二氧化碳无毒 | 两种分子中碳、氧原子的个数比不同 |
| A. | A | B. | B | C. | C | D. | D |
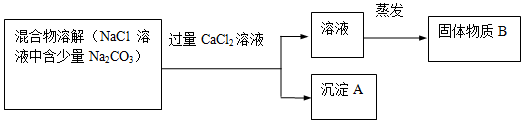
18.某实验小组的同学用氢氧化钠溶液和盐酸做中和反应的实验,当他们向盛有氢氧化钠溶液的烧杯中滴加一定量的稀盐酸后,发现忘记了滴加指示剂.他们停止滴加稀盐酸,对烧杯内溶液中的溶质成分进行探究.
(1)写出该中和反应的化学方程式:NaOH+HCl═NaCl+H2O.
(2)探究烧杯内溶液中的溶质的成分.
【猜想】猜想一:可能是NaCl和NaOH;猜想二:可能只有NaCl;
猜想三:可能是NaCl和HCl.
【进行实验】
(1)写出该中和反应的化学方程式:NaOH+HCl═NaCl+H2O.
(2)探究烧杯内溶液中的溶质的成分.
【猜想】猜想一:可能是NaCl和NaOH;猜想二:可能只有NaCl;
猜想三:可能是NaCl和HCl.
【进行实验】
| 实验步骤 | 实验操作 | 实验现象 | 结论 |
| ① | 取少量烧杯内的溶液于试管中,滴入几滴酚酞试液,振荡 | 溶液不变色 | 猜想一不成立 |
| ② | 取少量烧杯内的溶液于另一支试管中,滴加碳酸钠溶液 | 产生气泡 | 猜想三成立 |
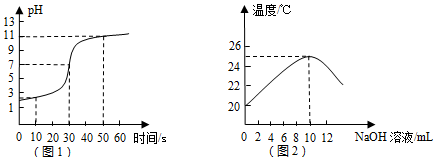
5.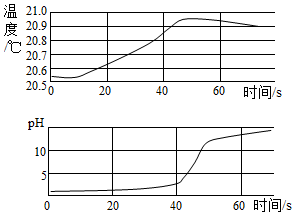 实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化.测定结果如图所示.下列说法不正确的是( )
实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化.测定结果如图所示.下列说法不正确的是( )
 实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化.测定结果如图所示.下列说法不正确的是( )
实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化.测定结果如图所示.下列说法不正确的是( )| A. | 反应过程中有热量放出 | |
| B. | 30s时,溶液中溶质为HCl和NaCl | |
| C. | 该实验是将稀盐酸滴入稀NaOH溶液 | |
| D. | 从20s到40s,溶液的温度升高、pH增大 |
3.正确的实验操作是安全地进行实验并获得可靠实验结果的前提.如图所示的实验操作,正确的是( )
| A. | 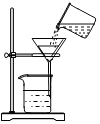 过滤 | B. | 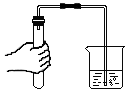 检查气密性 | C. | 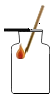 二氧化碳验满 | D. | 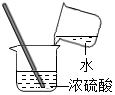 稀释浓硫酸 |