题目内容
2.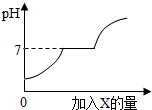 现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量的某物质X,溶液的pH随滴入X的量的变化关系如图所示,则X可能是( )
现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量的某物质X,溶液的pH随滴入X的量的变化关系如图所示,则X可能是( )| A. | 水 | B. | 纯碱溶液 | C. | 碳酸钙 | D. | 烧碱溶液 |
分析 首先根据溶液酸碱性的变化来推断所加物质的酸碱性,能够根据溶液酸碱性的变化来推断物质间的反应.
解答 解:由于随着X的加入溶液由酸性逐渐的变为中性又变为碱性,因此X应是一种碱性物质,首先排除水和氢氧化钠,再就是图象的中间一段溶液的PH值没有发生变化,说明X也能与氯化钙发生反应,
当把氯化钙也消耗完以后,再加X就会导致溶液变为碱性,碳酸钙与氯化钙不反应,所以X为纯碱溶液.
故选:B.
点评 本题主要考查了对图象的分析,能够根据图象来推断物质间的反应,培养学生分析问题、解决问题的能力.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
12.某同学为探究某种铜铁合金中铁的质量分数,先后在烧杯中进行了四次试验(杂质不与稀硫酸反应),实验数据如下表:
根据该同学的实验,试回答以下问题:
(1)上表第四次实验中合金里的铁恰好与稀硫酸完全反应,则其中X=150,Y=179.4.
(2)该铜铁合金中铁的质量分数.
(3)所加稀硫酸溶质质量分数(结果保留至0.1%).
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 所取合金的质量/g | 10 | 10 | 20 | 30 |
| 所加稀硫酸的质量/g | 80 | 100 | 50 | X |
| 反应后烧杯中剩余物质的质量/g | 89.8 | 109.8 | 69.8 | Y |
(1)上表第四次实验中合金里的铁恰好与稀硫酸完全反应,则其中X=150,Y=179.4.
(2)该铜铁合金中铁的质量分数.
(3)所加稀硫酸溶质质量分数(结果保留至0.1%).
10. 根据溶液有关知识,回答下列问题.
根据溶液有关知识,回答下列问题.
(1)生理盐水是质量分数为0.9%的氯化钠溶液.实验室若要配制生理盐水200g,应称取氯化钠固体1.8g,实验中要用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管.
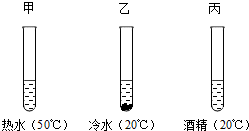
(2)在甲、乙、丙三支试管中各放入2gX晶体,再分别加入质量都为10.Og的热水、冷水、酒精,充分搅拌静置后,结果如图所示.
表 不同温度下NaCl和KNO3的溶解度
由图实验可知影响物质溶解性的因素有温度、溶剂的种类.实验中若将甲试管溶液降温至t1℃时,溶液恰好饱和,则t1℃,X的溶解度是20gg.若再往甲中加入5g水,改变温度至t2℃时,溶液又恰好饱和,则t1>t2(填“>”、“<”或“=”).
(3)根据表提供的信息用结晶的方法分离NaCl和KNO3的混合物.取100g混合物于100g热水中.完全溶解后,冷却至10℃,要得到纯净的KN03晶体,混合物中KN03的质量m的取值范围是85.5g>m>64.2g.
 根据溶液有关知识,回答下列问题.
根据溶液有关知识,回答下列问题.(1)生理盐水是质量分数为0.9%的氯化钠溶液.实验室若要配制生理盐水200g,应称取氯化钠固体1.8g,实验中要用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管.
(2)在甲、乙、丙三支试管中各放入2gX晶体,再分别加入质量都为10.Og的热水、冷水、酒精,充分搅拌静置后,结果如图所示.
表 不同温度下NaCl和KNO3的溶解度
| 温度/℃ | 10 | 30 | 50 | 70 | |
| 溶解度 /g | NaCl | 35.8 | 36.3 | 37.0 | 37.8 |
| KNO3 | 20.9 | 45.8 | 85.5 | 138 | |
(3)根据表提供的信息用结晶的方法分离NaCl和KNO3的混合物.取100g混合物于100g热水中.完全溶解后,冷却至10℃,要得到纯净的KN03晶体,混合物中KN03的质量m的取值范围是85.5g>m>64.2g.
17.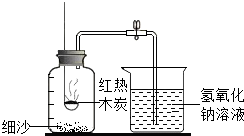 某研究性学习小组在“利用燃碳法测定空气中氧气的体积分数”的实验时(如图装置),发现一个现象:氢氧化钠溶液吸收生成的二氧化碳后,进入集气瓶中氢氧化钠溶液的体积分数仍然小于$\frac{1}{5}$.
某研究性学习小组在“利用燃碳法测定空气中氧气的体积分数”的实验时(如图装置),发现一个现象:氢氧化钠溶液吸收生成的二氧化碳后,进入集气瓶中氢氧化钠溶液的体积分数仍然小于$\frac{1}{5}$.
(1)写出氢氧化钠溶液吸收二氧化碳发生反应的化学方程式CO2+2NaOH=Na2CO3+H2O.
(2)教材中利用燃烧红磷法测定空气中氧气体积分数,选择该药品的原因是红磷只能与氧气反应且生成物为固体.
【提出问题】是什么原因导致测量不准确呢?
【猜想与假设】他们分别作了如下猜想:
甲同学:可能是木炭取的量过少;
乙同学:可能是木炭燃烧没有消耗完集气瓶中的氧气;
小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,都认为甲同学的猜想不合理.
【查阅资料】木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数高达14.0%、8.0%和16.0%.
乙同学又利用上述装置设计了如下实验,请你填写如表.
【交流与反思】
(3)请分析步骤2中,你选择的可燃物的理由三种物质燃烧时需要的氧气浓度大小依次为蜡烛>木炭>棉花.
(4)由此实验你对物质燃烧的条件有何新的认识可燃物燃烧需要的氧气要达到一定的浓度(或可燃物燃烧需要足够的氧气).
(5)从木炭燃烧反应的产物分析你认为测量结果小于$\frac{1}{5}$的理由还有可能是木炭燃烧生成了CO.
 某研究性学习小组在“利用燃碳法测定空气中氧气的体积分数”的实验时(如图装置),发现一个现象:氢氧化钠溶液吸收生成的二氧化碳后,进入集气瓶中氢氧化钠溶液的体积分数仍然小于$\frac{1}{5}$.
某研究性学习小组在“利用燃碳法测定空气中氧气的体积分数”的实验时(如图装置),发现一个现象:氢氧化钠溶液吸收生成的二氧化碳后,进入集气瓶中氢氧化钠溶液的体积分数仍然小于$\frac{1}{5}$.(1)写出氢氧化钠溶液吸收二氧化碳发生反应的化学方程式CO2+2NaOH=Na2CO3+H2O.
(2)教材中利用燃烧红磷法测定空气中氧气体积分数,选择该药品的原因是红磷只能与氧气反应且生成物为固体.
【提出问题】是什么原因导致测量不准确呢?
【猜想与假设】他们分别作了如下猜想:
甲同学:可能是木炭取的量过少;
乙同学:可能是木炭燃烧没有消耗完集气瓶中的氧气;
小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,都认为甲同学的猜想不合理.
【查阅资料】木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数高达14.0%、8.0%和16.0%.
乙同学又利用上述装置设计了如下实验,请你填写如表.
| 实验步骤 | 实验现象 | 实验结论 |
| 1将足量木炭点燃,迅速插入集气瓶中 | 棉花继续燃烧 | 木炭燃烧没有消耗完集气瓶中的氧气. |
| 2待冷却后,将燃着的棉花(填“棉花”或“蜡烛”)再伸入该集气瓶中 |
(3)请分析步骤2中,你选择的可燃物的理由三种物质燃烧时需要的氧气浓度大小依次为蜡烛>木炭>棉花.
(4)由此实验你对物质燃烧的条件有何新的认识可燃物燃烧需要的氧气要达到一定的浓度(或可燃物燃烧需要足够的氧气).
(5)从木炭燃烧反应的产物分析你认为测量结果小于$\frac{1}{5}$的理由还有可能是木炭燃烧生成了CO.
7.分离、提纯是化学实验的重要环节,下列实验设计不能达到实验目的是( )
| 选项 | 物质 | 杂质(少量) | 试剂及操作方法 |
| A | 一氧化碳 | 水蒸气和二氧化碳 | 先通过浓硫酸,再通过氢氧化钠溶液 |
| B | 氯化钠 | 碳酸钠 | 先加足量水溶解,再加适量稀盐酸,蒸发结晶 |
| C | 硝酸钾溶液 | 硫酸钾 | 加入适量的Ba(NO3)2溶液,过滤 |
| D | 铜粉 | 铁粉 | 用磁铁吸引 |
| A. | A | B. | B | C. | C | D. | D |
14.下列家庭小实验不能成功的是( )
| A. | 用燃烧的方法区别羊毛和涤纶 | B. | 用闻气味的方法区别白酒和白醋 | ||
| C. | 用食盐水浸泡菜刀除去表面的铁锈 | D. | 用肥皂水区别软水和硬水 |
11.下列对露置在空气中已部分变质的氢氧化钠溶液样品进行的相关实验中,实验现象及结论合理的是( )
| A. | 取一定量溶液样品,滴入适量的澄清石灰水,过滤,向滤液中滴加酚酞溶液,溶液变红,证明原样品中含有氢氧化钠 | |
| B. | 向溶液样品中加入适量的澄清石灰水至恰好完全反应,过滤,可除去样品中的杂质 | |
| C. | 取少量溶液样品,滴入氯化钡溶液,有白色沉淀生成 | |
| D. | 取一定量溶液样品,滴入稀盐酸,立即有大量气体产生 |
12.下列现象中属于化学变化的是( )
| A. | 石蜡熔化 | B. | 酒精挥发 | C. | 玻璃破碎 | D. | 钢铁生锈 |