题目内容
2.下列不易加快冰糖溶解的方法是( )| A. | 加水 | B. | 加热 | C. | 搅拌 | D. | 把冰糖粉碎 |
分析 只要能改变固体与水的接触机会就能改变固体的溶解速率;加快固体物质溶解速率的方法主要有:搅拌、加热、磨成粉末等,其中研成粉末状是为了增加溶质溶剂的接触面积.
解答 解:A、增加水的量,实际上是影响溶解溶质的量的多少,与溶解速率无关,故选项正确.
B、加热能加快分子运动速度,能加快食盐与水的接触机会,从而加快了食盐的溶解速率,故选项错误.
C、搅拌能加快分子运动速度,能加快食盐与水的接触机会,从而加快了食盐的速率速率,故选项错误.
D、固体颗粒大小决定了固体与水的接触面积的大小,也能改变溶解速率,把冰糖粉碎,增加了冰糖与水的接触面积,加快了固体的溶解速率,故选项错误.
故选:A.
点评 本题难度不大,考查了影响物质溶解速度的因素,了解影响物质溶解速率的因素(搅拌、加热、研磨等)即可正确解答本题.

练习册系列答案
相关题目
12.下列变化中,属于物理变化的是( )
| A. | 酒精燃烧 | B. | 镁条的燃烧 | C. | 蜡烛的熔化 | D. | 碱式碳酸铜受热 |
17.制作糕点常用Na2CO3或NaHCO3作膨松剂,我校化学兴趣小组的同学根据Na2CO3和NaHCO3的性质进行了一系列探究.
【查阅资料】
(1)溶解度比较:
(2)已知碳酸氢钠在270℃左右就能分解为碳酸钠、水和二氧化碳,而碳酸钠受热不分解.
(3)常温下,浓度相同的Na2 CO3溶液比NaHCO3溶液的碱性强.
【探究一】NaHCO3和Na2CO3性质差异的探究.
①验证水溶液的酸碱性的差异:分别测两种物质等浓度溶液的pH,请写出,测定pH的方法:将pH试纸放在表面皿上,用玻璃棒蘸取待测溶液滴在pH试纸上,然后与标准比色卡对照,读出pH.测定结果:NaHCO3溶液的pH<(填“>”或“<”)Na2CO3溶液.
②利用溶解度的差异鉴别NaHCO3和Na2CO3:小方同学分别取xg两种固体粉末加入20℃10g水中充分溶解,通过观察现象区分出碳酸钠和碳酸氢钠,x可能是A.
A.2 B.0.96 C.0.5 D.3
【探究二】测定某NaHCO3和Na2CO3混合物中NaHCO3的质量分数利用图①装置进行实验,装置B中放有样品(整套装置气密性良好,各装置中气体吸收剂足量).

【实验步骤】
(1)检查装置的气密性;(2)称取样品10g,加到装置B中;(3)称量装置B、C、D的质量(含药品);(4)连接装置;(5)加热;(6)停止加热继续通入空气;(7)再次称量装置B、C、D的质量(含药品).
【数据记录】
【问题回答】
①写出碳酸氢钠受热分解的化学方程式:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,B装置中盛样品的仪器名称是玻璃管.
②图1装置C的作用是吸收水蒸气,装置C中一个明显的错误是右侧导管伸入液面以下.
③实验过程中必须向装置内通入空气,装置A中发生反应的化学方程式为2NaOH+CO2=Na2CO3+H2O.若没有装置A,造成测定结果偏大(填“偏大”“不变”或“偏小”)
【讨论分析】小红同学认为,表格中三组数据都可以计算该样品中NaHCO3的质量分数,但小张认为不能用C装置的质量变化来计算,其理由是装置A中逸出的水蒸气会进入装置C中;改进方法:在装置A、B之间增加一个浓硫酸的干燥装置.小王又认为用装置D的质量差会偏大而影响计算,应增加一个操作:连接D装置前,缓缓鼓入空气,目的是排尽装置内的二氧化碳气体.
小陈经过认真思考,认为D中的气流会带出水蒸气,用装置D的质量差会偏小而影响计算,在D装置的右边需要再接上一个装置.他认为可以用图②两个中的一个,可老师认为最好选用其中的乙(填“甲”或“乙”)装置,其理由是碱石灰不仅能吸收D装置逸出的水蒸气,也能吸收D装置可能逸出的二氧化碳气体,与C装置整体计算,结果更准确(不考虑右侧空气的影响).经过反复讨论,大家一致赞成应该利用表格中的装置B的质量变化进行计算NaHCO3和Na2CO3混合物中NaHCO3的质量分数.(写出计算过程)
【查阅资料】
(1)溶解度比较:
| 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
(3)常温下,浓度相同的Na2 CO3溶液比NaHCO3溶液的碱性强.
【探究一】NaHCO3和Na2CO3性质差异的探究.
①验证水溶液的酸碱性的差异:分别测两种物质等浓度溶液的pH,请写出,测定pH的方法:将pH试纸放在表面皿上,用玻璃棒蘸取待测溶液滴在pH试纸上,然后与标准比色卡对照,读出pH.测定结果:NaHCO3溶液的pH<(填“>”或“<”)Na2CO3溶液.
②利用溶解度的差异鉴别NaHCO3和Na2CO3:小方同学分别取xg两种固体粉末加入20℃10g水中充分溶解,通过观察现象区分出碳酸钠和碳酸氢钠,x可能是A.
A.2 B.0.96 C.0.5 D.3
【探究二】测定某NaHCO3和Na2CO3混合物中NaHCO3的质量分数利用图①装置进行实验,装置B中放有样品(整套装置气密性良好,各装置中气体吸收剂足量).

【实验步骤】
(1)检查装置的气密性;(2)称取样品10g,加到装置B中;(3)称量装置B、C、D的质量(含药品);(4)连接装置;(5)加热;(6)停止加热继续通入空气;(7)再次称量装置B、C、D的质量(含药品).
【数据记录】
| 装置B | 装置C | 装置D | |
| 实验前物质的质量/g | 180.0 | 200.0 | 122.2 |
| 实验后物质的质量/g | 176.9 | 201.5 | 124.8 |
①写出碳酸氢钠受热分解的化学方程式:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,B装置中盛样品的仪器名称是玻璃管.
②图1装置C的作用是吸收水蒸气,装置C中一个明显的错误是右侧导管伸入液面以下.
③实验过程中必须向装置内通入空气,装置A中发生反应的化学方程式为2NaOH+CO2=Na2CO3+H2O.若没有装置A,造成测定结果偏大(填“偏大”“不变”或“偏小”)
【讨论分析】小红同学认为,表格中三组数据都可以计算该样品中NaHCO3的质量分数,但小张认为不能用C装置的质量变化来计算,其理由是装置A中逸出的水蒸气会进入装置C中;改进方法:在装置A、B之间增加一个浓硫酸的干燥装置.小王又认为用装置D的质量差会偏大而影响计算,应增加一个操作:连接D装置前,缓缓鼓入空气,目的是排尽装置内的二氧化碳气体.
小陈经过认真思考,认为D中的气流会带出水蒸气,用装置D的质量差会偏小而影响计算,在D装置的右边需要再接上一个装置.他认为可以用图②两个中的一个,可老师认为最好选用其中的乙(填“甲”或“乙”)装置,其理由是碱石灰不仅能吸收D装置逸出的水蒸气,也能吸收D装置可能逸出的二氧化碳气体,与C装置整体计算,结果更准确(不考虑右侧空气的影响).经过反复讨论,大家一致赞成应该利用表格中的装置B的质量变化进行计算NaHCO3和Na2CO3混合物中NaHCO3的质量分数.(写出计算过程)
14.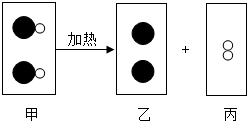 某反应的微观示意图如图所示,其中“●”表示汞原子,“○”表示氧原子,下列说法正确的是( )
某反应的微观示意图如图所示,其中“●”表示汞原子,“○”表示氧原子,下列说法正确的是( )
 某反应的微观示意图如图所示,其中“●”表示汞原子,“○”表示氧原子,下列说法正确的是( )
某反应的微观示意图如图所示,其中“●”表示汞原子,“○”表示氧原子,下列说法正确的是( )| A. | 图中甲、乙、丙三种物质中,甲、丙属于氧化物 | |
| B. | 图中甲、乙、丙三种物质均是由分子构成的 | |
| C. | 图中甲、乙、丙三种物质中既有单质又有化合物 | |
| D. | 该反应前后分子种类、原子种类均没有改变 |
12.走进花园能够闻到花香,下列对此现象的解释最合理的是( )
| A. | 分子间是有间隔的 | B. | 分子是不断运动的 | ||
| C. | 分子自身有能量 | D. | 分子是由原子构成的 |
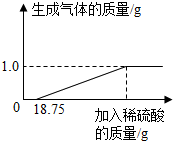 某兴趣小组对生锈废铁锅中铁的含量进行了测定.生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅等元素(除Fe、Fe2O3以外的物质都不与稀硫酸反应).兴趣小组的同学称取33g废铁锅片放入特制容器中,缓慢加入39.2%的稀硫酸,直到反应完全(假设硫酸先与表面的铁锈发生反应),实验数据如图所示.
某兴趣小组对生锈废铁锅中铁的含量进行了测定.生锈的铁锅中除Fe、Fe2O3外,还含有碳、硅等元素(除Fe、Fe2O3以外的物质都不与稀硫酸反应).兴趣小组的同学称取33g废铁锅片放入特制容器中,缓慢加入39.2%的稀硫酸,直到反应完全(假设硫酸先与表面的铁锈发生反应),实验数据如图所示. 根据下列粒子结构示意图,回答问题
根据下列粒子结构示意图,回答问题