题目内容
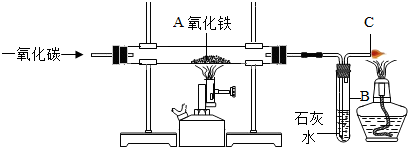
5.在“实验室制取气体并验证气体性质”的实验课中,小红同学欲用图1所示的装置制取二氧化碳并验证二氧化碳的性质.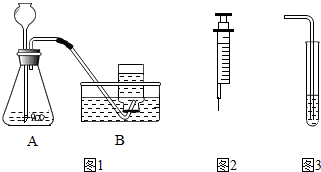
(1)若按图1装置操作,有明显错误,此错误是:不能用排水法收集二氧化碳气体,理由为二氧化碳能溶于水.
(2)为了便于控制反应的进行,可用图2所示注射器代替图1装置A中的长颈漏斗(填仪器名称).
(3)用装置A制取二氧化碳有关反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.
(4)为了验证产生的气体为二氧化碳,小红同学将装置A与图3的装置相连,若试管中的试剂为澄清石灰水,观察到的现象是澄清石灰水变浑浊.但是小红错将氢氧化钠溶液倒入试管中,观察不到现象;为了证明产生的二氧化碳气体也能与氢氧化钠溶液发生反应,请你设计一个方案:取少量液体于试管中,滴加稀盐酸,观察到有气泡产生,证明二氧化碳与氢氧化钠溶液发生了反应(简述实验步骤、现象和结论).
(5)利用图1中所示的发生装置A,还可用来制取的气体有O2(合理均可)(写一种),选用的反应试剂是过氧化氢与二氧化锰.
分析 (1)据二氧化碳能溶于水分析解答;
(2)注射器可控制滴加液体的速度,进而可控制反应速率;
(3)实验室制取二氧化碳用大理石和稀盐酸,据反应原理书写方程式;
(4)二氧化碳能使澄清的石灰水变浑浊,二氧化碳与氢氧化钠反应会生成碳酸钠,要验证二氧化碳是否与氢氧化钠发生了反应,可验证是否有碳酸根;
(5)图1发生装置属于固液常温型,可用来制取氧气或氢气,据此分析解答.
解答 解:(1)二氧化碳能溶于水,不能用排水法收集,操作错误;
(2)注射器可控制滴加液体的速度,进而可控制反应速率,所以可用注射器代替长颈漏斗控制反应进行;
(3)实验室制取二氧化碳用大理石和稀盐酸,二者反应生成氯化钙、水和二氧化碳,反应方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)二氧化碳通入澄清的石灰水会使之变浑浊;因为二氧化碳与氢氧化钠反应会生成碳酸钠,要验证二氧化碳是否与氢氧化钠发生了反应,可验证是否有碳酸根,故可向B实验后的溶液中加入足量稀盐酸,若观察到有气泡产生,就可以证明二氧化碳与氢氧化钠发生了反应;
(5)图1发生装置属于固液常温型,可用来制取氧气或氢气,若用来制取氧气,使用的药品是过氧化氢和二氧化锰,若用来制取氢气,使用的药品是锌粒和稀硫酸;
故答案为:(1)不能用排水法收集二氧化碳气体; 二氧化碳能溶于水;
(2)长颈漏斗;
(3)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)澄清石灰水变浑浊; 取少量液体于试管中,滴加稀盐酸,观察到有气泡产生,证明二氧化碳与氢氧化钠溶液发生了反应;
(5)O2(合理均可); 过氧化氢; 二氧化锰.
点评 了解实验室制取二氧化碳的原理、二氧化碳的性质及氧气、氢气的制法是解答此题的关键,能较好考查学生对知识的掌握和运用能力.

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案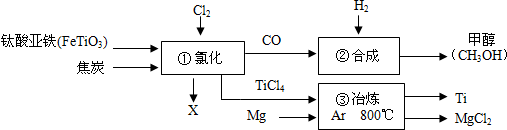
| A. | ?中氩气(Ar)作反应物 | |
| B. | 钛酸亚铁(FeTiO3)中钛元素为+3价 | |
| C. | ②中为使原料全部转化为甲醇,理论上CO和H2的质量比为14:1 | |
| D. | ①中反应为:2FeTiO3+6C+7Cl2═2X+2TiCl4+6CO,则X为FeCl3 |
【提出猜想】CO2与Na反应可能生成4种物质:C、CO、Na2O、Na2CO3.
【查阅资料】①Na是非常活泼的金属,常温下与O2、H2O等物质反应.
②Na2O是白色固体,与H2O反应生成NaOH.
③向氯化钯(PdCl2)溶液中通入CO,产生黑色沉淀.
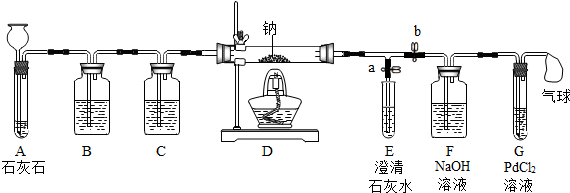
【实验过程】同学们在老师的指导下设计了如图所示装置(部分夹持仪器已略去)
【实验记录】
| 序号 | 实验操作 | 主要实验现象 | 实验结论和解释 |
| ① | 打开a,关闭b,由长颈漏斗注入稀盐酸 | A中产生大量气泡 E中出现浑浊 | E中反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O. |
| ② | 当E中出现浑浊时,打开b,关闭a,点燃酒精灯 | D中Na剧烈燃烧,产生白烟,内壁附着黑色、白色固体 G中产生黑色沉淀 | 反应产物一定有C和CO |
| ③ | 取D中白色固体于试管中,加水溶解,再加入石灰水 | 产生白色沉淀 | 反应产物还有Na2CO3. |
①实验记录②中,E中出现浑浊,再点燃酒精灯的目的排出装置中的空气,防止空气的干扰.
②检验第4种物质是否存在的实验方案:取D中白色固体于试管中,加水完全溶解,加入过量CaCl2溶液至不再产生沉淀,滴加酚酞试液,溶液呈红色.说明白色固体中含Na2O.
| A. | 墙内开花墙外香------分子在不停运动 | |
| B. | 25m3的石油气在加压情况下可装入容积为0.024m3的钢瓶中-----分子间有间隔 | |
| C. | 湿衣服在阳光下比阴凉处易晾干------温度高时分子运动,温度低时分子不运动 | |
| D. | 干冰和二氧化碳都可以用于灭火-------分子相同,化学性质相同 |