题目内容
16.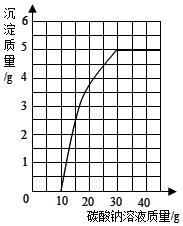 实验室用过量的稀盐酸和大理石制取CO2,待反应后过滤,称得滤液质量为25g,向其中逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.回答下列问题:
实验室用过量的稀盐酸和大理石制取CO2,待反应后过滤,称得滤液质量为25g,向其中逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.回答下列问题:(1)从图中可以看出生成沉淀最大质量是5g
(2)开始加入碳酸钠溶液至10g时,还没有沉淀析出的原因是碳酸钠先与盐酸反应,然后再与氯化钙反应,所以开始反应不会生成沉淀;
(3)计算原滤液中氯化钙的质量分数.
分析 (1)根据图示信息找出沉淀的最大质量;
(2)根据稀盐酸过量,故加入碳酸钠后首先与过量的稀盐酸反应,然后再与氯化钙反应进行解答;
(3)根据沉淀的最大质量可求出原滤液中氯化钙的质量,然后根据溶质的质量分数的计算方法计算质量分数.
解答 解:(1)由图可以看出,生成沉淀的最大质量是5g;
(2)因稀盐酸过量,故加入碳酸钠后首先与过量的稀盐酸反应,然后再与氯化钙反应,所以开始反应不会生成沉淀;
(3)设原滤液中CaCl2的质量为x
Na2CO3+CaCl2=CaCO3↓+2NaCl
111 100
x 5g
$\frac{111}{100}=\frac{x}{5g}$
x=5.55g
故原滤液中氯化钙的质量分数为:$\frac{5.55g}{25g}$×100%=22.2%
故答案为:(1)5;
(2)碳酸钠先与盐酸反应,然后再与氯化钙反应,所以开始反应不会生成沉淀;
(3)NaCl和Na2CO3;(4)原滤液中氯化钙的质量分数是22.2%.
点评 此题是对物质分析及图象识别考查题,解题的关键是能对表格及图象有明确的认识,解决此题对培养学生良好的分析问题的能力有一定帮助.

练习册系列答案
相关题目
6.区分日常生活中的下列各组物质,所加试剂或操作方法完全正确的是( )
| 需区分的物质 | 方法1 | 方法2 | |
| A | 碳酸钠溶液和氯化钠溶液 | 分别加入石蕊溶液 | 分别加足量氯化钙溶液 |
| B | 食盐水和蒸馏水 | 分别测两种液体的pH | 分别加热蒸发 |
| C | 氧化铁和氧化铜 | 分别观察固体的颜色 | 分别加入足量的稀硫酸 |
| D | 一氧化碳和二氧化碳 | 分别闻气体气味 | 分别通过灼热的氧化铜 |
| A. | A | B. | B | C. | C | D. | D |
11.下列实验设计能达到实验目的是( )
| 序号 | 实验目的 | 实验方案 |
| A | 稀释浓硫酸 | 将水缓慢加入浓硫酸中,并搅拌 |
| B | 除去K2SO4溶液中的KOH | 加入适量稀盐酸 |
| C | 检验某气体是否为二氧化碳 | 用燃着的木条 |
| D | 区分氧化钙与碳酸钙 | 取样品,加入适量水 |
| A. | A | B. | B | C. | C | D. | D |
8.下列没有发生化学反应的是( )
| A. | 蓄电池放电 | B. | 水力发电 | C. | 内燃机做功冲程 | D. | 火箭点火升空 |
5.现有60℃的饱和硝酸钾溶液,欲降低其溶质质量分数,下列方法可行的是( )
| A. | 加入一定量的硝酸钾 | B. | 恒温蒸发部分水 | ||
| C. | 升温到80℃ | D. | 加入一定量的氯化钠 |
6.下列化学用语书写正确的是( )
| A. | 3个硫酸根离子:3SO4-2 | |
| B. | 2个镁原子:Mg2 | |
| C. | 五氧化二磷分子:O2P5 | |
| D. | 标出氯化钙中氯元素的化合价:Ca$\stackrel{-1}{C{l}_{2}}$ |