题目内容
1911年著名物理学家卢瑟福在用一束带正电的、质量比电子大得多的高速运动的α粒子轰击金箔时发现:①大多数α粒子能穿透金箔而不改变原来的运动方向;②少部分α粒子改变原来的方向,发生偏转;③极少数的 粒子被反弹了回来。由此不能推出关于原子内部结构的信息是
粒子被反弹了回来。由此不能推出关于原子内部结构的信息是

A. 原子核体积很小
B. 原子核带正电
C. 原子内部有“很大”的空间
D. 原子只有一个原子核
D

 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案生活中处处有化学。
(1)下表为某品牌燕麦片的主要成分。
| 每100g含有的营养成分 | 糖 类 | 油 脂 | 蛋白质 | 维生素C | 钙 | 钠 | 锌 |
| 7.6g | 7.8g | 7.4g | 18mg | 201mg | 30.8mg | 8.1mg |
表中没有列出的营养素是 ▲ ,若缺少表中的 ▲ 元素会造成骨质疏松。
(2)用洗涤剂清洗油污,是利用了洗涤剂的 ▲ 作用。
(3)在厨房中能用来除去水壶中水垢的物质是 ▲ (填“食醋”或“食盐水”)。
(4)炎热的夏季自行 车车胎容易爆裂, 从微观角度分析原因是 ▲ 。
车车胎容易爆裂, 从微观角度分析原因是 ▲ 。
(5)下图所示的各种厨房用品的主要材料 ,属于有机合成材料的是 ▲ 。
,属于有机合成材料的是 ▲ 。

(6)煮汤时,取少量汤进行品尝就可知道整锅汤咸味如何,是因为溶液具有 ▲ (填写一条性质)。
(7)目前常用硬币都是合金制造的,这些合金具有的一条性质是 ▲ 。
化学课外兴趣活动小组的同学对某炼铁厂生产的生铁进行组成分析。取生铁样品与足量的稀
| 反应前 | 反应后 | ||
| 实验数据 | 稀盐酸的质量 | 生铁样品的质量 | 反应后烧杯中混合物的质量 |
| 200 g | 14.5 g | 214.0 g |
盐酸在烧杯中反应(假设生铁中的杂质不与酸反应,也不溶于水),其实验数据如下表:(有关反的化学方程式为:Fe + 2HCl= FeCl2 + H2↑)(1)根据质量守恒定律可知,反应中生成的氢气的质量为_______ g。(2)计算该生铁样品中铁的质量分数
为防止面粉加工厂发生爆炸,应张贴的标志是( )
|
| A. |
| B. |
| C. |
| D. |
|
 2的质量、10g铝与足量盐酸反应生成H2的质量
2的质量、10g铝与足量盐酸反应生成H2的质量 B. 表示乳酸由碳、氢、氧三种元素组成
B. 表示乳酸由碳、氢、氧三种元素组成 . 表示乳酸这种物质
. 表示乳酸这种物质 原子、3个氧原子构成
原子、3个氧原子构成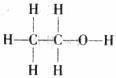 。乙醇是无色、透明、有香味、易挥发的液体,密度比水小,熔点-117.3℃,沸点78.5℃,极易溶于水。具有可燃性,能与金属钠发生反应生成氢气。依据上述信息回答下列问题:
。乙醇是无色、透明、有香味、易挥发的液体,密度比水小,熔点-117.3℃,沸点78.5℃,极易溶于水。具有可燃性,能与金属钠发生反应生成氢气。依据上述信息回答下列问题: (右下角方框内填上原子个数);
(右下角方框内填上原子个数);


