题目内容
16.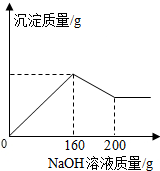 已知氢氧化铝能溶解在过量的氢氧化钠溶液中生成偏铝酸钠(NaAlO2)溶液,有关化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O.现有160.0g某无色溶液,可能含有盐酸、硫酸镁、硫酸铜、氯化铝中的一种或数种.取100.0g该溶液于烧杯中,往其中逐滴加入20.0%的NaOH溶液,产生沉淀的质量与加入NaOH溶液的质量关系如图所示.下列判断合理的是( )
已知氢氧化铝能溶解在过量的氢氧化钠溶液中生成偏铝酸钠(NaAlO2)溶液,有关化学方程式为:Al(OH)3+NaOH═NaAlO2+2H2O.现有160.0g某无色溶液,可能含有盐酸、硫酸镁、硫酸铜、氯化铝中的一种或数种.取100.0g该溶液于烧杯中,往其中逐滴加入20.0%的NaOH溶液,产生沉淀的质量与加入NaOH溶液的质量关系如图所示.下列判断合理的是( )| A. | 一定有AlCl3、MgSO4和CuSO4 | |
| B. | 一定有AlCl3和MgSO4,一定没有盐酸 | |
| C. | 一定有AlCl3和MgSO4,可能有盐酸 | |
| D. | 一定有AlCl3和CuSO4,可能有MgSO4 |
分析 因为溶液是无色的,因此溶液中不含有硫酸铜;
稀盐酸能和氢氧化钠反应生成氯化钠和水,硫酸镁和氢氧化钠反应生成氢氧化镁沉淀和硫酸钠,氯化铝和氢氧化钠反应生成氢氧化铝沉淀和氯化钠,氢氧化铝能溶解在过量的氢氧化钠溶液中生成偏铝酸钠和水.
解答 解:A、因为溶液是无色的,因此溶液中一定不含有硫酸铜,该选项说法不正确;
B、因为一开始就产生沉淀,说明溶液中不含有稀盐酸,当加入160g氢氧化钠溶液后继续加入氢氧化钠溶液时,沉淀减少,说明反应生成的氢氧化铝沉淀在溶解,进一步说明溶液中含有氯化铝,当加入200g氢氧化钠溶液后沉淀不再减少,说明溶液中一定含有硫酸镁,最终没有溶解的沉淀是硫酸镁和氢氧化钠反应生成的氢氧化镁,该选项说法正确;
C、如果溶液中含有稀盐酸时,则氢氧化钠先和稀盐酸反应生成氯化钠和水,因此开始不能产生沉淀,该选项说法不正确;
D、溶液中一定不含有硫酸铜,这是因为硫酸铜溶液是蓝色溶液,该选项说法不正确.
故选:B.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
6.NH3和Cl2混合可发生下列化学反应:2NH3+3Cl2=6HCl+N2,该反应的基本类型是( )
| A. | 化合反应 | B. | 分解反应 | C. | 复分解反应 | D. | 置换反应 |
11.某学习小组同学讨论辨析以下说法:①均一、稳定、透明的液体都是溶液;②分子可分,原子不可分;③pH<6.5的降水称为酸雨;④生成盐和水的反应不一定是中和反应;⑤糖类、油脂、蛋白质是人体必须的营养物质,均能为人体提供能量;⑥混合物中至少有2种元素.其中正确的是( )
| A. | ④⑤ | B. | ①②③⑥ | C. | ③④⑤⑥ | D. | ①②③④⑤⑥ |
5.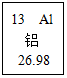 如图是元素周期表中的一种元素,下列有关该元素的信息正确的是( )
如图是元素周期表中的一种元素,下列有关该元素的信息正确的是( )
 如图是元素周期表中的一种元素,下列有关该元素的信息正确的是( )
如图是元素周期表中的一种元素,下列有关该元素的信息正确的是( )| A. | 原子序数是13 | B. | 它是非金属元素 | ||
| C. | 其原子的原子核内有13个中子 | D. | 相对原子质量是26.98g |
6.用“ ”和“
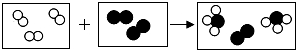
”和“ ”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物X,微观过程如图所示,下列说法正确的是( )
”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物X,微观过程如图所示,下列说法正确的是( )
 ”和“
”和“ ”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物X,微观过程如图所示,下列说法正确的是( )
”分别代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生化学反应生成新物X,微观过程如图所示,下列说法正确的是( )
| A. | 在反应过程中A2和B2分子保持不变 | |
| B. | 该反应为置换反应 | |
| C. | 参加反应的A2与B2分子数之比为3:1 | |
| D. | 物质X含4种元素 |
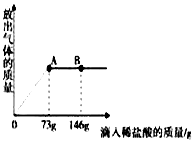 在一烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,加入109.1g水溶解,制成溶液.向其中滴加溶质质量分数10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系如图所示,请回答问题:
在一烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,加入109.1g水溶解,制成溶液.向其中滴加溶质质量分数10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系如图所示,请回答问题: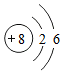 有A、B、C、D四种元素,A元素组成的单质是最常见的金属;B元素的原子结构示意图如图所示;C元素的单质是最清洁的燃料;D元素是地壳中含量最多的金属元素.则:A元素是铁;B的离子符号是O2-;C的单质是氢气;B、C、D三种元素组成的化合物是Al(OH)3.
有A、B、C、D四种元素,A元素组成的单质是最常见的金属;B元素的原子结构示意图如图所示;C元素的单质是最清洁的燃料;D元素是地壳中含量最多的金属元素.则:A元素是铁;B的离子符号是O2-;C的单质是氢气;B、C、D三种元素组成的化合物是Al(OH)3.