题目内容
1.二氧化碳能产生温室效应,还能作化工原料.(1)化石燃料燃烧会产生大量的CO2,天然气(CH4)充分燃烧的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
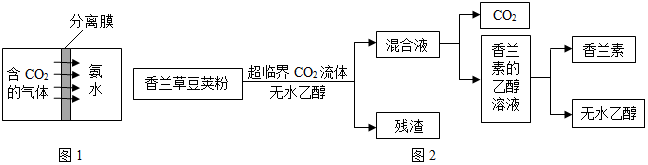
(2)膜分离是一种常用的分离技术.二氧化硅(SiO2)能用于制造CO2分离膜,CO2通过此膜后被氨水吸收(如图1所示),转化为可作氮肥的NH4HCO3.
①SiO2中硅元素的化合价为+4.
②NH4HCO3固体中氮元素的质量分数为17.7%(计算结果精确到0.1% ).
(3)CO2形成的超临界CO2流体可用于从香兰草豆荚粉中提取香兰素(C8H8O3)(如图2).
①以上提取香兰素的过程中,可循环使用的物质有无水乙醇和CO2.
②完全燃烧19g香兰素所生成的二氧化碳与完全燃烧23g无水乙醇(俗名酒精,C2H5OH)所生成的二氧化碳的质量相等.
分析 (1)根据反应物和生成物及其质量守恒定律可以书写化学方程式.
(2)①根据二氧化硅的化学式为SiO2,利用氧化物中氧元素的化合价及化合物中元素的正负化合价的代数和为0来计算其中硅元素的化合价;
②根据化合物中元素的质量分数进行分析;
(3)①根据题中信息解答;
②根据化学式进行计算即可
解答 解:(1)天然气的主要成分是甲烷,甲烷燃烧的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.故答案为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)①在二氧化硅中,氧元素的化合价为-2价,
设硅元素的化合价为x,
由化学式为SiO2,根据化合物中元素的正负化合价的代数和为0,则
x+(-2)×2=0
解得:x=+4;
②碳酸氢铵中氮元素的质量分数=$\frac{14}{14+1×5+12+16×3}×100%$≈17.7%;故填:+4;17.7%;
(3)①根据图示可知可循环使用的物质有CO2,无水乙醇;故填:CO2;
②二氧化碳的质量相等也就是所含碳元素的质量相等.根据质量守恒定律可知,也就是香兰素中碳元素的质量与乙醇中碳元素的质量相等.
设乙醇的质量为x,则
19g×$\frac{12×8}{12×8+1×8+16×3}$×100%=x×$\frac{12×2}{12×2+1×6+16}$×100%
x=23g
故填:23.
点评 本题考查化合价的计算,学生应熟悉常见元素的化合价,尤其注意氧化物中氧元素的化合价,并能用化合价计算的原则来进行计算.本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
12.某同学将一小包铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到固体和蓝色溶液,并对滤液的组成进行探究.
(1)锌和硝酸银反应的化学方程式是Zn+2AgNO3═Zn(NO3)2+2Ag;
(2)同学们对滤液中所含的溶质做出多种猜想.其中有两种猜想可能成立,这两种猜想是:
猜想一:硝酸铜和硝酸锌 猜想二硝酸锌、硝酸铜和硝酸银
(3)请你设计一种方案 来验证猜想二成立.
(1)锌和硝酸银反应的化学方程式是Zn+2AgNO3═Zn(NO3)2+2Ag;
(2)同学们对滤液中所含的溶质做出多种猜想.其中有两种猜想可能成立,这两种猜想是:
猜想一:硝酸铜和硝酸锌 猜想二硝酸锌、硝酸铜和硝酸银
(3)请你设计一种方案 来验证猜想二成立.
| 实验步骤 | 现象 | 结论 |
| 取样,加过量稀盐酸 | 产生白色沉淀 | 猜想二成立 |
9.如图所示实验不能达到实验目的是( )
| A. | 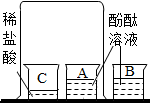 探究分子的运动 | B. | 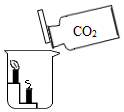 证明密度比空气大 | ||
| C. | 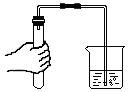 检查装置的气密性 | D. |  比较合金 和纯金属的硬度 |
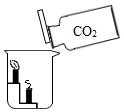 如图所示,将集气瓶中的二氧化碳气体沿烧杯壁倒入烧杯中,看到下层的蜡烛先熄灭,由此实验可以证明二氧化碳的性质是:①密度比空气大;②不燃烧、不支持燃烧,从而推测CO2可以用来灭火.
如图所示,将集气瓶中的二氧化碳气体沿烧杯壁倒入烧杯中,看到下层的蜡烛先熄灭,由此实验可以证明二氧化碳的性质是:①密度比空气大;②不燃烧、不支持燃烧,从而推测CO2可以用来灭火.
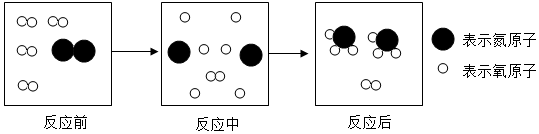
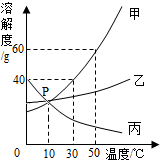 甲、乙、丙三种固体物质在水中的溶解度曲线如图所示.请回答:
甲、乙、丙三种固体物质在水中的溶解度曲线如图所示.请回答: 根据如图回答有关问题:有上、下两个集气瓶中分别盛有空气和红棕色的二氧化碳气体,当抽出玻璃片后,过一会儿,可观察到什么现象?请用分子的观点解释这一现象.
根据如图回答有关问题:有上、下两个集气瓶中分别盛有空气和红棕色的二氧化碳气体,当抽出玻璃片后,过一会儿,可观察到什么现象?请用分子的观点解释这一现象.