题目内容
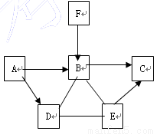
(15分)(1)实验室若用氯酸钾制取氧气,可选用下图的发生装置是 (填序号),反应的化学方程式为 __________________;

(2)小李用一定溶质质量分数的过氧化氢溶液和二氧化锰固体制取并收集一瓶干燥的氧气,正确的组装顺序为 。(填字母)
(3)用C装置通过复分解反应制取某种气体,应选用的液体药品是___________,反应的化学方程式为 ;检验此气体的反应的化学方程式为 。
(4)人们使用天然气(主要成分为甲烷)过程中要注意通风,如果氧气不足会产生一氧化碳,使人中毒。某兴趣小组在实验室利用下列实验装置,在老师指导下制取氧气和甲烷,并检验甲烷燃烧后的气体产物。
①小王用无水醋酸钠(化学式为CH3COONa)和碱石灰固体混合加热制取甲烷,
发生装置应选择上图中的 (填字母),并写出无水醋酸钠与碱石灰中的氢氧化钠反应生成甲烷和碳酸钠的化学方程式 。
②下面是小张对甲烷在氧气中燃烧后的气体产物进行验证的实验。(假定每步均完全反应)
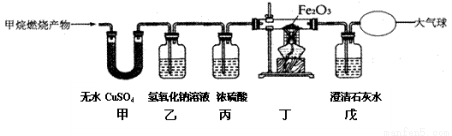
(温馨提示:无水硫酸铜吸水后变蓝,常用于吸收水和验证水的存在;丁装置中酒精灯的网罩起集中火焰升高温度的作用。)
请回答:①如果将甲、乙装置顺序进行交换,则不能验证燃烧产物中的 ;
②完成实验报告
实验操作 | 实验现象 | 实验结论 |
将燃烧后的气体产物进行验证 | 甲中的白色固体变蓝 | 燃烧产物中有_________ |
乙装置质量增加 | 燃烧产物中有_________ | |
丁中玻璃管内固体颜色变化是 、戊中澄清石灰水变浑浊 | 燃烧产物中有CO 写出丁中玻璃管内反应的化学方程式 |
③实验结束,对相关装置进行称量(忽略空气成分对实验的干扰):甲装置增重3.6g,乙装置增重2.2g。那么燃烧甲烷的质量为 g,并写出该实验中甲烷燃烧的化学方程式 。
.(1)A 2KClO3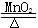 2KCl+3O2↑ 略 (2)CFD (3)稀盐酸;CaCO3+ 2 HCl == CaCl2 + CO2↑+ H2O;CO2 + Ca(OH)2 = CaCO3↓+ H2O
2KCl+3O2↑ 略 (2)CFD (3)稀盐酸;CaCO3+ 2 HCl == CaCl2 + CO2↑+ H2O;CO2 + Ca(OH)2 = CaCO3↓+ H2O
(4)① A CH3COONa+NaOH CH4↑+Na2CO3 回答 ①. H2O ②完成实验报告:H2O CO2;3CO +Fe2O3高温2 Fe + 3 CO2;③. 1.6 4CH4+7O2
CH4↑+Na2CO3 回答 ①. H2O ②完成实验报告:H2O CO2;3CO +Fe2O3高温2 Fe + 3 CO2;③. 1.6 4CH4+7O2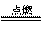 2CO2+2CO+8H2O
2CO2+2CO+8H2O
【解析】
试题分析:(1)实验室用氯酸钾和二氧化锰的混合物加热制取氧气,所以应该选用固固加热型发生装置,化学方程式为:2KClO3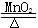 2KCl+3O2↑;(2)制取并得到干燥的装置为:CFD;(3)用C装置通过复分解反应制取二氧化碳,则选用的液体药品为稀盐酸,用大理石或石灰石与稀盐酸反应制取二氧化碳,检验二氧化碳用澄清的石灰水。(4)①根据反应物的状态和反应条件知,应选用固固加热型发生装置,根据文字叙述可知化学方程式为:CH3COONa+NaOH
2KCl+3O2↑;(2)制取并得到干燥的装置为:CFD;(3)用C装置通过复分解反应制取二氧化碳,则选用的液体药品为稀盐酸,用大理石或石灰石与稀盐酸反应制取二氧化碳,检验二氧化碳用澄清的石灰水。(4)①根据反应物的状态和反应条件知,应选用固固加热型发生装置,根据文字叙述可知化学方程式为:CH3COONa+NaOH CH4↑+Na2CO3;请回答:①如果将甲、乙装置顺序进行交换,则不能验证燃烧产物中的水,②完成实验报告:甲中的白色固体变为蓝色,证明燃烧产物有水;丁中固体颜色由红棕色变为黑色,一氧化碳和氧化铁在高温条件下生成铁和二氧化碳,化学方程式为:3 CO +Fe2O3高温2 Fe + 3 CO2③实验结束:根据质量守恒定律,化学反应前后元素质量保持不变,可知水中氢元素质量=3.6g*(2/18*100%)=0.4g;二氧化碳中碳元素质量=4.4g*(12/44*100%)=1.2g,则甲烷的质量=0.4g+1.2g=1.6g。根据题意知,化学方程式为:4CH4+7O2
CH4↑+Na2CO3;请回答:①如果将甲、乙装置顺序进行交换,则不能验证燃烧产物中的水,②完成实验报告:甲中的白色固体变为蓝色,证明燃烧产物有水;丁中固体颜色由红棕色变为黑色,一氧化碳和氧化铁在高温条件下生成铁和二氧化碳,化学方程式为:3 CO +Fe2O3高温2 Fe + 3 CO2③实验结束:根据质量守恒定律,化学反应前后元素质量保持不变,可知水中氢元素质量=3.6g*(2/18*100%)=0.4g;二氧化碳中碳元素质量=4.4g*(12/44*100%)=1.2g,则甲烷的质量=0.4g+1.2g=1.6g。根据题意知,化学方程式为:4CH4+7O2 2CO2+2CO+8H2O
2CO2+2CO+8H2O
考点:气体的实验室制法,气体燃烧成分的确定。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案为除去下表样品中的少量杂质(括号内为杂质),所选试剂及操作方法均正确的是
序号 | 样品成分 | 所选试剂 | 操作方法 |
A | KCl(MnO2) | 水 | 溶解、过滤、洗涤、干燥 |
B | Na2CO3(NH4HCO3) | 加热至质量不再减少 | |
C | NaCl(KNO3) | 水 | 溶解、降温结晶、过滤 |
D | NaCl(CuCl2) | 过量NaOH溶液 | 过滤、蒸发结晶 |