题目内容
2.某混合液里可能含有NaNO3、NaCl、Na2CO3、Na2SO4中的一种或几种,取少量这种溶液分别盛放于两支试管中,进行如下实验:(1)向第一支试管中逐滴加入稀硝酸时,溶液生成无色气体,该气体能使澄清石灰水变浑浊,继续加入稀硝酸使溶液显酸性时,再加入硝酸钡溶液不产生沉淀.
(2)向第二支试管中加入过量硝酸钡溶液时生成白色沉淀,进行过滤,在滤液滴加硝酸银溶液出现白色沉淀.
据实验推断:溶液中肯定含有NaCl、Na2CO3.如果把第(2)步所加过量硝酸钡溶液改为“过量氯化钡溶液”,不能验证的物质是NaCl.
分析 (1)硝酸钠、氯化钠、碳酸钠、硫酸钠四种物质中,能与稀硝酸放出无色气体的只有碳酸钠,碳酸钠与盐酸反应生成氯化钠、水和二氧化碳;继续加入稀硝酸使溶液显酸性时,再加入硝酸钡溶液不产生沉淀,说明没有硫酸钠,因为产生的硫酸钡沉淀不溶于稀硝酸;
(2)向第二支试管中加入过量硝酸钡溶液时生成碳酸钡白色沉淀,进行过滤,在滤液滴加硝酸银溶液出现白色沉淀,说明含有氯化钠,据此分析.
解答 解:(1)硝酸钠、氯化钠、碳酸钠、硫酸钠四种物质中,能与稀硝酸放出无色气体的只有碳酸钠,碳酸钠与盐酸反应生成氯化钠、水和二氧化碳;继续加入稀硝酸使溶液显酸性时,再加入硝酸钡溶液不产生沉淀,说明没有硫酸钠,因为产生的硫酸钡沉淀不溶于稀硝酸;
(2)向第二支试管中加入过量硝酸钡溶液时生成碳酸钡白色沉淀,进行过滤,在滤液滴加硝酸银溶液出现白色沉淀,说明含有氯化钠,无法判断硝酸钠的存在;因此:
据实验推断:溶液中肯定含有NaCl、Na2CO3;因为氯化钡会引入氯离子,对氯化钠中的氯离子检验会产生干扰,因此如果把第(2)步所加过量硝酸钡溶液改为“过量氯化钡溶液”,不能验证的物质是NaCl;
故答案为:NaCl、Na2CO3;NaCl.
点评 根据物质的性质或变化规律,结合实验探究中每步实验所出现的现象,对混合物的可能组成进行分析、判断,最终形成结论.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
12.下列有关实验现象的描述正确的是( )
| A. | 硫在空气中燃烧发出明亮的蓝紫色火焰 | |
| B. | 铁丝在氧气中剧烈燃烧生成四氧化三铁 | |
| C. | 红磷在氧气中燃烧产生大量白雾 | |
| D. | 生锈的铁钉投入稀盐酸中溶液变成黄色 |
13.元素间的区别主要决定于原子的( )
| A. | 核电荷数 | B. | 中子数 | C. | 相对原子质量 | D. | 电子层数 |
10.除去下列物质中含有的少量杂质(括号内为杂质),所用试剂及主要操作均合理的是( )
| 选项 | 物质 | 所用试剂或方法 |
| A | N2(O2) | 木炭、点燃 |
| B | KCl(MnO2) | 溶解、过滤、蒸发结晶 |
| C | FeSO4溶液(CuSO4) | 锌粒、过滤 |
| D | NaCl溶液(Na2SO4) | Ba(NO3)2溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
17.下列图示实验操作中,正确的是( )
| A. | 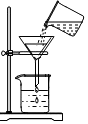 过滤粗盐溶液 | B. | 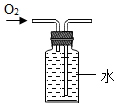 收集氧气 | ||
| C. | 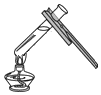 加热溶液 | D. | 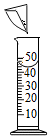 将NaCl倒入量筒中配制溶液 |
14.把一定质量的氯化钾饱和溶液通过一种措施使之变成不饱和溶液,下列说法中正确的是( )
| A. | 溶剂质量可能不变 | B. | 溶液中溶质的质量分数一定减小 | ||
| C. | 溶液质量一定增大 | D. | 溶液中溶质的质量分数可能增大 |
11.物质的分离方法很多,下列两种物质的混合物,你认为可以用过滤方法除去的是( )
| A. | 酒精和水 | B. | 泥沙和蔗糖 | C. | 硝酸钾和水 | D. | 铜粉和铁粉 |
 A、B、C、D、E分别是氧化铁、铁、氧气、一氧化碳、盐酸中的一种物质,请回答下列问题:
A、B、C、D、E分别是氧化铁、铁、氧气、一氧化碳、盐酸中的一种物质,请回答下列问题: