题目内容
9.下列物质属于前者属于化合物,后者属于单质的一组( )| A. | 空气 氢气 | B. | 二氧化碳 氮气 | ||
| C. | 过氧化氢 水 | D. | 高锰酸钾 稀有气体 |
分析 单质是由一种元素组成的纯净物,化合物是由不同种元素组成的纯净物.
解答 解:A、空气是混合物,错误;
B、二氧化碳是化合物,氮气是单质,正确;
C、过氧化氢和水都是化合物,错误;
D、高锰酸钾是化合物,稀有气体是混合物,错误;
故选B
点评 判断纯净物和混合物时,就是判断物质的物质组成;判断是否是单质、化合物、氧化物时,既要判断元素组成,又要判断物质组成.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案
相关题目
2.某同学测定硫酸铜晶体(CuSO4•5H2O)里结晶水的含量,请回答下列问题:
(1)实验步骤为:①研磨 ②称量空坩埚和装有试样的坩埚的质量 ③加热 ④冷却 ⑤称量 ⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止 ⑦根据实验数据计算硫酸铜结晶水的含量.现有坩埚、坩埚钳、三脚架、泥三角、研钵、玻璃棒、干燥器、药匙、酒精灯、火柴、硫酸铜晶体样品等实验用品,进行该实验时,缺少的实验用品是托盘天平.实验步骤⑥的目的是使硫酸铜晶体中的结晶水完全失去.
(2)细心的同学发现在加热硫酸铜晶体时,会闻到刺激性气味,那分解的产物是什么呢?
查阅资料发现:硫酸铜受热分解生成氧化铜和气体,气体是由SO2、SO3、O2中的一种或几种;SO2、SO3都能被碱石灰(氢氧化钠和氧化钙混合物)吸收,SO2、SO3都能被氢氧化钠溶液吸收.同学利用如图装置探究硫酸铜受热分解生成的气体的成分(假设加热硫酸铜粉末直至完全分解).实验结果发现:用带火星的木条伸入集气瓶D,发现木条能复燃,说明气体中含有O2.已知硫酸铜粉末质量为10.0克,完全分解后,各装置的质量变化关系如下表所示:
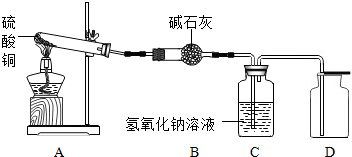
请通过计算,推断出该实验条件下硫酸铜分解的化学方程式是哪一个?B
A.3CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$3CuO+SO3↑+2SO2↑+O2↑ B.4CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$4CuO+2SO3↑+2SO2↑+O2↑
C.5CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$5CuO+SO3↑+4SO2↑+2O2↑ D.6CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$6CuO+4SO3↑+2SO2↑+O2↑
(1)实验步骤为:①研磨 ②称量空坩埚和装有试样的坩埚的质量 ③加热 ④冷却 ⑤称量 ⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止 ⑦根据实验数据计算硫酸铜结晶水的含量.现有坩埚、坩埚钳、三脚架、泥三角、研钵、玻璃棒、干燥器、药匙、酒精灯、火柴、硫酸铜晶体样品等实验用品,进行该实验时,缺少的实验用品是托盘天平.实验步骤⑥的目的是使硫酸铜晶体中的结晶水完全失去.
(2)细心的同学发现在加热硫酸铜晶体时,会闻到刺激性气味,那分解的产物是什么呢?
查阅资料发现:硫酸铜受热分解生成氧化铜和气体,气体是由SO2、SO3、O2中的一种或几种;SO2、SO3都能被碱石灰(氢氧化钠和氧化钙混合物)吸收,SO2、SO3都能被氢氧化钠溶液吸收.同学利用如图装置探究硫酸铜受热分解生成的气体的成分(假设加热硫酸铜粉末直至完全分解).实验结果发现:用带火星的木条伸入集气瓶D,发现木条能复燃,说明气体中含有O2.已知硫酸铜粉末质量为10.0克,完全分解后,各装置的质量变化关系如下表所示:

| 装置 | A(试管+粉末) | B | C |
| 反应前 | 42.0克 | 75.0克 | 140.0克 |
| 反应后 | 37.0克 | 79.5克 | 140.0克 |
A.3CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$3CuO+SO3↑+2SO2↑+O2↑ B.4CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$4CuO+2SO3↑+2SO2↑+O2↑
C.5CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$5CuO+SO3↑+4SO2↑+2O2↑ D.6CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$6CuO+4SO3↑+2SO2↑+O2↑
20.下列做法中,你认为不利于改善我市空气质量的是( )
| A. | 就地焚烧植物的秸杆和垃圾 | B. | 植树种花,搞好绿化 | ||
| C. | 使用清洁能源 | D. | 安装机动车辆尾气净化装置 |
4.如图为元素周期表中氟元素的相关信息,下列说法错误的是( )


| A. | 氟原子核内质子数为9 | B. | 氟元素为非金属元素 | ||
| C. | 氟元素的相对原子质量为19g | D. | 氟元素符号为F |
1.正确的实验操作对实验结果,人身安全都非常重要.下列实验操作不正确的是( )
| A. | 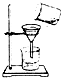 过滤 | B. |  取固体粉末 | C. |  熄灭酒精灯 | D. | 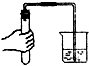 检查气密性 |
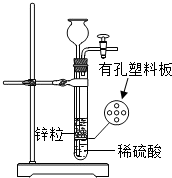 图为实验室制取氢气的发生装置.若液面刚好不与锌粒接触而又无酸液可加,要得到氢气且不影响氢气的制取量,可从长颈漏斗中加入适量试剂的一组是( )
图为实验室制取氢气的发生装置.若液面刚好不与锌粒接触而又无酸液可加,要得到氢气且不影响氢气的制取量,可从长颈漏斗中加入适量试剂的一组是( )