题目内容
(1)自来水厂常用的净水的方法有沉淀、____________、吸附、消毒等。
在电解水的实验中,常向水中加入某种强电解质(如NaOH)等,其目的是_______;
写出水通电分解的化学方程式__________________。
(2)能源和环境与人类的生产生活密切相关.
a.氢能是未来最理想的能源,从环保角度分析,氢能最突出的优点是______。目前,氢氧燃料电池已经被应用,氢氧燃料电池是一种将化学能转化为______能的装置。
b.汽车尾气是导致酸雨的重要原因。在汽油中加入适量乙醇作为汽车燃料,可减少汽车尾气的污染。乙醇汽油是___________(填“混合物”或“纯净物”)。
 过滤;增强水的导电性;2H2O 2H2↑+ O2↑燃烧产物是水,无污染;电; .混合物
【解析】
(1)自来水厂常用的净水的方法有沉淀、过滤、吸附、消毒等;在电解水的实验中,常向水中加入某种强电解质,其目的是增强水的导电性;水通电分解成氧气和氢气,其化学方程式为2H2O 2H2↑+ O2↑;
(2)
a、氢能是未来最理想的能源,从环保角度分析,氢气燃烧后生成水,没有污染;氢...
过滤;增强水的导电性;2H2O 2H2↑+ O2↑燃烧产物是水,无污染;电; .混合物
【解析】
(1)自来水厂常用的净水的方法有沉淀、过滤、吸附、消毒等;在电解水的实验中,常向水中加入某种强电解质,其目的是增强水的导电性;水通电分解成氧气和氢气,其化学方程式为2H2O 2H2↑+ O2↑;
(2)
a、氢能是未来最理想的能源,从环保角度分析,氢气燃烧后生成水,没有污染;氢...
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案下列有关物质用途的说法中,错误的是
A. 食盐用作调味剂 B. 石灰石用作建筑材料
C. 小苏打用作补钙剂 D. 熟石灰用于改良酸性土壤
 C
【解析】
物质的性质决定物质的用途,只要熟悉所给物质的性质,答案很容易得出。
A、食盐具有咸味,可作调味剂,正确;B、石灰石常用作建筑材料,正确;C、小苏打是碳酸氢钠,不含有钙元素,不能作补钙剂,错误;D、熟石灰显碱性,可用于改良酸性土壤,正确。故选C。
C
【解析】
物质的性质决定物质的用途,只要熟悉所给物质的性质,答案很容易得出。
A、食盐具有咸味,可作调味剂,正确;B、石灰石常用作建筑材料,正确;C、小苏打是碳酸氢钠,不含有钙元素,不能作补钙剂,错误;D、熟石灰显碱性,可用于改良酸性土壤,正确。故选C。 试管是化学实验中最常用的玻璃仪器.在不同的实验中,试管的放置方法是不同的.最常见的放置方法有如图六种.那么,在下列化学实验基本操作中,试管的放置方法分别是(填序号):

(1)给试管的固体加热:______.
(2)往试管里加入块状固体:______.
(3)给试管里的液体加热:______.
(4)往试管里倾倒液体:______.
(5)往试管里滴加液体:______.
(6)洗涤后的试管放置:______.
 FEDCAB
【解析】
(1)给试管的固体加热时,试管口要略微向下倾斜;
(2)往试管里加入块状固体药品时,先将试管横放;
(3)给试管里的液体加热时,试管与桌面成45度角;
(4)往试管里倾倒液体时,试管口要略微倾斜;
(5)往试管里滴加液体时,试管要直立;
(6)洗涤后的试管要倒放在试管架上。
FEDCAB
【解析】
(1)给试管的固体加热时,试管口要略微向下倾斜;
(2)往试管里加入块状固体药品时,先将试管横放;
(3)给试管里的液体加热时,试管与桌面成45度角;
(4)往试管里倾倒液体时,试管口要略微倾斜;
(5)往试管里滴加液体时,试管要直立;
(6)洗涤后的试管要倒放在试管架上。 下列关于空气各成分的说法中,正确的是( )
A. 氧气的化学性质比较活泼,能够燃烧
B. 空气中氮气的质量分数为78%
C. 稀有气体都不能与物质发生化学反应
D. 氮气的化学性质不活泼,可用于食品防腐
 D
【解析】
A、氧气能支持燃烧,具有助燃性,不具有可燃性,不能燃烧,故选项错误;B、空气中氮气的体积分数为78%,不是质量分数,故选项错误;C、稀有气体在一定的特殊条件下,可与一些物质发生化学反应,故选项错误;D、氮气的化学性质稳定,无毒,可用于食品防腐,故选项正确。故选D。
D
【解析】
A、氧气能支持燃烧,具有助燃性,不具有可燃性,不能燃烧,故选项错误;B、空气中氮气的体积分数为78%,不是质量分数,故选项错误;C、稀有气体在一定的特殊条件下,可与一些物质发生化学反应,故选项错误;D、氮气的化学性质稳定,无毒,可用于食品防腐,故选项正确。故选D。 某同学进行如下图的两个实验。

(l)甲实验观察到的现象是________________,溶液由蓝色变成无色。
(2)乙实验中反应的化学方程式为___________;
(3)把甲、乙反应后的溶液倒入同一烧怀,发现有白色沉淀生成。他决定对白色沉淀的成分进行探究。
(查阅资料)硫酸钡不溶于酸。
(提出猜想)白色沉淀为:Ⅰ.________Ⅱ.Mg(OH)和BaSO4;Ⅲ. Mg(OH)2和MgCO3.
(实验方案)
实验操作 | 实验现象与结论 |
过滤、洗涤白色沉淀备用;向白色沉淀中加入盐酸至过量 | ①沉淀全部溶解,且无其它现象;猜想Ⅰ成立;其化 学反应方程式为 ________________________。 ②若_________________且无气体产生,猜想Ⅱ成立。 ③若沉淀完全溶解,_______________,猜想Ⅲ成立。 |
(拓展与思考)如果猜想Ⅲ成立,产生此结果的原因是做乙实验时______________;
上述白色沉淀的成分不可能出现的组合是Mg(OH)2、MgCO3和BaSO4,原因是________________。
 镁条表面有红色物质析出;Na2CO3 + Ba(OH)2=== BaCO3↓+2NaOHMg(OH)2Mg(OH)2+2HCl===MgCl2+2H2O沉淀部分溶解有气体产生Na2CO3过量;Ba(OH)2和Na2CO3不可能同时剩余
【解析】
(1)镁能和硫酸铜反应生成铜和硫酸镁,故镁条表面有红色物质析出,溶液由蓝色变为无色;
(2)碳酸钠和氢氧化钡反应生成碳酸钡白色沉淀和氢氧...
镁条表面有红色物质析出;Na2CO3 + Ba(OH)2=== BaCO3↓+2NaOHMg(OH)2Mg(OH)2+2HCl===MgCl2+2H2O沉淀部分溶解有气体产生Na2CO3过量;Ba(OH)2和Na2CO3不可能同时剩余
【解析】
(1)镁能和硫酸铜反应生成铜和硫酸镁,故镁条表面有红色物质析出,溶液由蓝色变为无色;
(2)碳酸钠和氢氧化钡反应生成碳酸钡白色沉淀和氢氧... 实验室中有两瓶已失去标签的稀盐酸和氯化钠溶液,下列试剂中不能将其鉴别出来的是
A. 石蕊溶液 B. 锌粒 C. 碳酸钠溶液 D. 硝酸银溶液
 D
【解析】
A、稀盐酸显酸性,氯化钠显中性,故可用石蕊溶液鉴别,选项正确;B、稀盐酸可与锌反应生成气体氢气,氯化钠和锌不反应,可进行鉴别,选项正确;C、稀盐酸可与碳酸钠反应生成二氧化碳气体,氯化钠和碳酸钠不反应,故可进行鉴别,选项正确;D、稀盐酸和氯化钠均不与硝酸银溶液反应,故不能进行鉴别,选项错误。故本题选D。
D
【解析】
A、稀盐酸显酸性,氯化钠显中性,故可用石蕊溶液鉴别,选项正确;B、稀盐酸可与锌反应生成气体氢气,氯化钠和锌不反应,可进行鉴别,选项正确;C、稀盐酸可与碳酸钠反应生成二氧化碳气体,氯化钠和碳酸钠不反应,故可进行鉴别,选项正确;D、稀盐酸和氯化钠均不与硝酸银溶液反应,故不能进行鉴别,选项错误。故本题选D。 “缉毒犬”能够辨别气味,发现毒品的主要原因是
A. 分子体积很小 B. 分子可以分为原子
C. 分子间有间隔 D. 分子在不断运动
 D
【解析】
“缉毒犬”能够辨别气味,是因为毒品分子在不断运动,运动到空气中被“缉毒”犬发现,故本题选D。
D
【解析】
“缉毒犬”能够辨别气味,是因为毒品分子在不断运动,运动到空气中被“缉毒”犬发现,故本题选D。 用下图所示的简易净水器处理浑浊的河水,下面分析正确的是( )
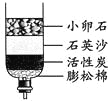
A. 净水器能杀菌消毒
B. 净化后的水属于纯净物
C. 活性炭的主要作用是吸附
D. 净水器能将硬水变为软水
 C
【解析】
试题过滤能除去水中的固体不溶物,不能杀菌消毒,且溶于水的物质不能通过过滤除去;将硬水软化的方法有煮沸、蒸馏等,过滤不能软化硬水。活性炭有吸附作用,能吸附水中的异味和色素。
C
【解析】
试题过滤能除去水中的固体不溶物,不能杀菌消毒,且溶于水的物质不能通过过滤除去;将硬水软化的方法有煮沸、蒸馏等,过滤不能软化硬水。活性炭有吸附作用,能吸附水中的异味和色素。 某学生用250 mL的集气瓶收集4瓶氧气,进行硫、红磷、木炭、铁丝的燃烧实验。
(1)写出铁丝在氧气中燃烧的实验现象:___________________________。
(2)写出红磷在氧气中燃烧的化学方程式:_______________。
(3)若要制取本实验所需的4瓶氧气(O2=1.43g/L),至少需要氯酸钾___克。(精确到0.01g)
 剧烈燃烧,火星四射,生成黑色固体,放出大量的热4P+5O2 2P2O53.65
【解析】
(1)铁丝在氧气中燃烧的实验现象:剧烈燃烧,火星四射,生成黑色固体,放出大量的热;
(2)红磷在氧气中燃烧生成五氧化二磷,化学方程式为:P+5O22P2O5 ;
(3)氧气质量为:4×0.25×1.43=1.43g,设至少需要氯酸钾的质量x,则:
剧烈燃烧,火星四射,生成黑色固体,放出大量的热4P+5O2 2P2O53.65
【解析】
(1)铁丝在氧气中燃烧的实验现象:剧烈燃烧,火星四射,生成黑色固体,放出大量的热;
(2)红磷在氧气中燃烧生成五氧化二磷,化学方程式为:P+5O22P2O5 ;
(3)氧气质量为:4×0.25×1.43=1.43g,设至少需要氯酸钾的质量x,则: 
