题目内容
(1)按以下要求写方程式:
①有水生成的氧化还原反应
②有水生成的非氧化还原反应
(2)四种基本反应类型中,肯定是氧化还原反应的类型是 ,可能是氧化还原反应类型的还有 .
①有水生成的氧化还原反应
②有水生成的非氧化还原反应
(2)四种基本反应类型中,肯定是氧化还原反应的类型是
考点:书写化学方程式、文字表达式、电离方程式,反应类型的判定
专题:化学用语和质量守恒定律
分析:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答:解:有元素化合价升降的反应属于氧化还原反应.
(1)①氢气与氧化铜反应生成铜和水,属于氧化还原反应,反应的化学方程式为:H2+CuO
Cu+H2O(合理即可).
②氢氧化钠与盐酸反应生成氯化钠和水,属于复分解反应,反应前后元素的化合价不变,不是有水生成的非氧化还原反应,反应的化学方程式为:NaOH+HCl=NaCl+H2O(合理即可).
(2)置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,一定有元素化合价变化,一定是氧化还原反应.
化合反应、分解反应可能有元素化合价升降,可能属于氧化还原反应,如4Al+3O2
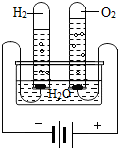
2Al2O3、2H2O
2H2↑+O2↑;复分解反应反应前后,元素的化合价不变,一定不是氧化还原反应.
故答案为:(1)①H2+CuO
Cu+H2O;②NaOH+HCl=NaCl+H2O等(合理即可).
(2)置换反应;化合反应、分解反应.
(1)①氢气与氧化铜反应生成铜和水,属于氧化还原反应,反应的化学方程式为:H2+CuO
| ||
②氢氧化钠与盐酸反应生成氯化钠和水,属于复分解反应,反应前后元素的化合价不变,不是有水生成的非氧化还原反应,反应的化学方程式为:NaOH+HCl=NaCl+H2O(合理即可).
(2)置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,一定有元素化合价变化,一定是氧化还原反应.
化合反应、分解反应可能有元素化合价升降,可能属于氧化还原反应,如4Al+3O2
| ||
| ||
故答案为:(1)①H2+CuO
| ||
(2)置换反应;化合反应、分解反应.
点评:本题难度不大,掌握化学方程式的书写方法、氧化还原反应的特征是正确解答本题的关键.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
中秋时节,丹桂飘香.从分子的角度,认识正确的是( )
| A、分子很小 |
| B、分子在不停地运动 |
| C、分子间存在间隔 |
| D、分子能保持物质的化学性质 |
氧气是一种化学性质比较活泼的气体,它可以与许多物质发生化学反应,如图所示.关于三个反应叙述中不正确的是( )
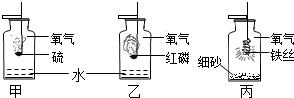

| A、都是化合反应 |
| B、反应都需要点燃;都放出热量 |
| C、甲中生成物是气体,乙、丙中生成物是固体 |
| D、甲中水和丙中细砂的作用完全一样 |
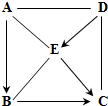 A、B、C、D、E分别是初中化学常见的五种化合物,其相互反应和转化关系如图所示(“-”表示两物质能反应,“→”表示转化关系,部分生成物及反应条件已略去).其中D、E均由两种元素组成,且不含相同元素.试回答下列问题:
A、B、C、D、E分别是初中化学常见的五种化合物,其相互反应和转化关系如图所示(“-”表示两物质能反应,“→”表示转化关系,部分生成物及反应条件已略去).其中D、E均由两种元素组成,且不含相同元素.试回答下列问题: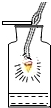
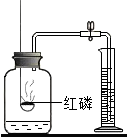
 所示,该元素原子的核电荷数为
所示,该元素原子的核电荷数为