题目内容
将20g生锈的铁片放入50g稀盐酸中,恰好完全反应,放出气体的质量为0.4g,试求:
(1)铁片中单质铁的质量;
(2)铁片中铁锈的质量分数;
(3)最后所得溶液的质量.
| 根据化学反应方程式的计算. | |
| 专题: | 有关化学方程式的计算. |
| 分析: | 由生成氢气的质量根据铁与盐酸反应的化学方程式可以计算出铁的质量,从而 |
| 解答: | 解: (1)设铁的质量为x. Fe+2HCl=FeCl2+H2↑ 56 2 x 0.4g
x=11.2g (2)原铁片上铁锈的质量是20﹣11.2g=8.8g 铁片中铁锈的质量分数 (3)最后所得溶液的质量为20g+50g﹣0.4g=69.6g 答案: (1)铁片中单质铁的 (2)铁片中铁锈的质 (3)最后所得溶液的质量69.6g |
| 点评: | 本题主要考查含杂质物质的化学方程式计算,难度稍大.做题时必须分析清楚所得溶液的质量和溶质的质量,学生做题时往往求错所得溶液的质量要理清所得溶液的质量就是反应前物质的质量和减去生成的氢气的质量只要理清这一点不难解答该类题目. |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列说法不正确的是( )
|
| A. | 燃烧不一定有火焰产生 |
|
| B. | 物质跟氧气的反应就是燃烧 |
|
| C. | 物质在有限的空间内燃烧,可能会引起爆炸 |
|
| D. | 物质燃烧的剧烈程度与氧气的浓度有关 |
下列对某一主题的知识归纳,有错误的是
| A.化学与安全 | B.化学与材料 |
| 重金属中毒—可喝鲜牛奶解毒 煤气泄漏—应关闭气阀、开窗通风 | 水泥、玻璃—都是无机材料 玻璃钢、铝合金—都是金属材料 |
| C.化学与食品 | D.化学与健康 |
| 蛋白质、淀粉—用碘酒可鉴别 糖类、油脂—组成元素相同 | 缺锌—易得侏儒症 缺铁—易得贫血症 |
 求出铁片中铁锈的质量,再根据质量守恒定律求出所得溶液的质量.
求出铁片中铁锈的质量,再根据质量守恒定律求出所得溶液的质量.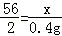
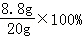 =44%
=44%