题目内容
9.某兴趣小组利用下列装置进行实验,请回答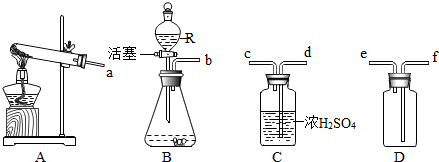
(1)R仪器的名称是分液漏斗,用过氧化氢制氧气应选用的发生装置是B (填序号,下同),分解过氧化氢制得的氧气常带有少量水蒸气,欲收集一瓶干燥的氧气,经过的导气管口正确的连接顺序是b、d、c、f、e
(2)若B装置中装有石灰石和稀盐酸,则该装置可用于制取CO2气体.收集该气体时通常用向上排空气法收集.制这种气体的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)若用加热高锰酸钾的方法制取氧气,需在 A 装置试管口放一团棉花,其化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
分析 本题主要考查制取氧气、二氧化碳的原理、装置、收集方法,以及仪器连接、气体干燥和化学方程式书写.解答时要结合所学的知识和实验经验,经分析后要有针对性地回答.气体制备装置的选择要考虑反应物的状态和反应条件,有固固加热型和固液常温型;选择收集气体的方法时要考虑气体在水中的溶解性和气体与空气密度的相对大小,有排水集气法和向上排空气法、向下排空气法.
解答 解:(1)R仪器叫做分液漏斗,它可以控制液体逐滴地滴下,有利于控制反应速度,用过氧化氢制氧气,选择B装置较好,用浓硫酸干燥氧气时,要求气体从长管进,短管出,若用D装置收集氧气,由于氧气密度比空气大,所以要求氧气f 进入,因此各导管连接口的顺序是b、d、c、f、e;
(2)石灰石的主要成分是碳酸钙,与盐酸反应生成二氧化碳气体,由于二氧化碳密度比空气大得多,通常用向上排空气法收集,该反应可用化学方程式表示为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)若用高锰酸钾制氧气,可选A装置,为了防止高锰酸钾小晶粒进入导管,常在试管口放一团棉花,该反应可用化学方程式表示为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
故答案是:
(1)分液漏斗、B;b、d、c、f、e;
(2)CO2、向上排空气、CaCO3+2HCl=CaCl2+H2O+CO2↑;
(3)一团棉花、2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
点评 本题尽管考查的知识内容不难,但由于考查的方式由整体选择变成化整为零地组合,需要对实验十分熟悉,没有经验是做不好的,另外本题在氧气的干燥和收集时,一定要把连接的顺序搞懂,需要打破常规思维.

| A. | 质子数相同的微粒,一定是同种元素 | |
| B. | 若A是可溶性碱,B是可溶性盐,则C和D可能是两种沉淀(A+B→C+D) | |
| C. | 在同一温度下,饱和溶液一定比不饱和溶液溶质质量分数大 | |
| D. | 若A、B各取10克,混合后使其反应,则C、D的质量总和一定等于20克(A+B→C+D) |
| A. | 3H---3个氢元素 | B. | C60---60个碳原子 | ||
| C. | $\stackrel{+3}{Fe}$---铁的化合价显+3价 | D. | NaCO3---碳酸钠 |
| A. | 全透明铝应该属于纯净物 | B. | 全透明铝也可能应用于手机屏幕 | ||
| C. | 全透明铝中原子不运动 | D. | 全透明铝与普通铝的化学性质不同 |
| A. | 大力开采矿物,保障金属材料的使用 | |
| B. | 推广利用太阳能、风能,缓解温室效应 | |
| C. | 采用焚烧的方法处理农作物秸秆和垃圾 | |
| D. | 生活中尽量使用含磷洗衣粉便于给水体提供养分 |
| A. | 含有氧元素的化合物一定是氧化物 | |
| B. | 原子核中一定有质子和中子 | |
| C. | 由同种分子构成的物质一定是纯净物 | |
| D. | 向不饱和溶液中加入足量该溶质一定能形成饱和溶液 |
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别硝酸钠溶液和硫酸钾溶液 | 取样,滴加Ba(NO3)2溶液,观察现象 |
| B | 检验二氧化碳中是否混有水蒸气 | 将混合气体通过无水硫酸铜 |
| C | 除去氯化钠溶液中的氯化钙 | 先加入过量碳酸钠溶液,过滤;再向滤液中加入适量稀盐酸,调节溶液的pH=7 |
| D | 探究镁、银、铜三种金属的活动 性强弱 | 将两根光亮的镁条分别伸入硫酸铜溶液和硝酸银溶液中 |
| A. | A | B. | B | C. | C | D. | D |
 化学与生活息息相关
化学与生活息息相关 表示氧原子,
表示氧原子, 表示铜原子,
表示铜原子, 表示氢原子.
表示氢原子.