题目内容
14. (1)如右图所示,量筒内液体的读数为42.0ml.
(1)如右图所示,量筒内液体的读数为42.0ml.(2)一同学平视量筒内液体体积为25mL,倒出部分液体后,俯视读数为11mL,则他倒出的实际液体体积大于(填“大于”“小于”或“等于”)14mL.
(3)某同学在称量物体质量时,把物体和砝码放倒了,最后读数为13.4克,则该同学所称物体的实际质量是6.6g(5克以下用游码).
分析 (1)根据题目中图可以看出从40~50之间分成了10个刻度,每个刻度是1mL,从下向上数字变大,可得出液体的体积为42mL进行分析;
(2)根据平视量筒内液体体积为25mL,读数正确,倒出部分液体后,俯视读数为11mL,实际剩余的体积小于11mL进行分析;
(3)根据天平正确使用时,物体质量=砝码质量+游码质量,左物右码放反了,物体质量=砝码质量-游码质量进行分析.
解答 解:(1)从题目中图可以看出从40~50之间分成了10个刻度,每个刻度是1mL,从下向上数字变大,可得出液体的体积为42mL;
(2)平视量筒内液体体积为25mL,读数正确,倒出部分液体后,俯视读数为11mL,实际剩余的体积小于11mL,所以倒出的实际液体体积大于14mL;
(3)天平正确使用时,物体质量=砝码质量+游码质量,左物右码放反了,物体质量=砝码质量-游码质量,所以所称物体的实际质量是:10g-3.4g=6.6g.
故答案为:(1)42.0ml;
(2)大于;
(2)6.6g.
点评 量筒的使用是中考热之一,量筒正确的读数方法和错误操作造成何种误差是必须掌握的基本内容.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
4. 某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成,取四份样品分别加稀硫酸反应,其实验数据记录如下表.
某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成,取四份样品分别加稀硫酸反应,其实验数据记录如下表.
试计算:
(1)经分析,在第1、2两份样品测得的数据中,硫酸(填物质名称)完全反应了.
(2)列式计算黄铜屑样品中的锌的质量分数.
(3)请在图中画出在100.0g样品中加稀硫酸的质量与产生气体质量变化关系的示意图.(请注意图象的转折点所在)
 某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成,取四份样品分别加稀硫酸反应,其实验数据记录如下表.
某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成,取四份样品分别加稀硫酸反应,其实验数据记录如下表. | 样品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品质量(g) | 100.0 | 100.0 | 100.0 | 100.0 |
| 取稀硫酸质量(g) | 200.0 | 400.0 | 600.0 | 800.0 |
| 产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
(1)经分析,在第1、2两份样品测得的数据中,硫酸(填物质名称)完全反应了.
(2)列式计算黄铜屑样品中的锌的质量分数.
(3)请在图中画出在100.0g样品中加稀硫酸的质量与产生气体质量变化关系的示意图.(请注意图象的转折点所在)
5.在氢气、水、氯化氢三种物质中都含有( )
| A. | 都含氢分子 | B. | 都含有氢气 | C. | 都含有氢原子 | D. | 都含有氢元素 |
2.能在水中大量共存的一组离子是( )
| A. | K+、Na+、Cl-、SO42- | B. | H+、Na+、Cl-、CO32- | ||
| C. | Ag+、Cu2+、Cl-、SO42- | D. | Na+、Ca2+、OH-、CO32- |
3.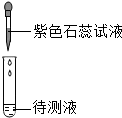 实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.
实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.
(1)甲同学的实验中向稀盐酸中滴加石蕊试液后,溶液颜色为红色.
(2)甲组同学将两支试管中的液体混合后,烧杯A中的溶液溶质一定有BC(选填序号).
A.HCl B.NaOH C.NaCl
(3)两位同学继续对烧杯C中的废液成分进行探究:
【猜想与假设】通过分析上述实验现象,烧杯C中的废液除石蕊和水外,其组成可能为:
①NaCl和NaOH ②NaCl、NaOH、Ca(OH)2 ③NaOH、NaCl、Na2CO3.
【设计完成实验】请设计实验验证烧杯C中的废液可能的组成:
(4)最后,两位同学向烧杯C中加入适量的稀盐酸,实现了此次实验的绿色排放(呈中性).
 实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.
实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.(1)甲同学的实验中向稀盐酸中滴加石蕊试液后,溶液颜色为红色.
(2)甲组同学将两支试管中的液体混合后,烧杯A中的溶液溶质一定有BC(选填序号).
A.HCl B.NaOH C.NaCl
(3)两位同学继续对烧杯C中的废液成分进行探究:
【猜想与假设】通过分析上述实验现象,烧杯C中的废液除石蕊和水外,其组成可能为:
①NaCl和NaOH ②NaCl、NaOH、Ca(OH)2 ③NaOH、NaCl、Na2CO3.
【设计完成实验】请设计实验验证烧杯C中的废液可能的组成:
| 操作方法 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,向其中滴加足量的稀盐酸 | 有气泡产生 | 猜想③成立 |
 如图所示,其中X、Y、Z、R、E分别是氧化铁、氯化钠溶液、稀硫酸、氢氧化钡溶液、碳酸钠溶液、二氧化碳中的一种.图中短线相连的物质间均能相互发生反应,已知X和R反应生成气体Y.
如图所示,其中X、Y、Z、R、E分别是氧化铁、氯化钠溶液、稀硫酸、氢氧化钡溶液、碳酸钠溶液、二氧化碳中的一种.图中短线相连的物质间均能相互发生反应,已知X和R反应生成气体Y.