题目内容
通过一年的化学学习,我们掌握了一些气体的制备方法,例如制取氧气的方法有:A.分离空气 B.加热分解高锰酸钾 C.分解过氧化氢 D.加热分解氯酸钾 E.电解水等等.也熟悉一些气体的制取和收集装置,例如: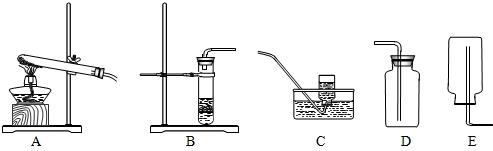
(1)以上制取氧气的方法中,只发生了物理变化的是
(2)如用方法C制取氧气的化学反应方程式是
(3)实验室制备并收集二氧化碳应选的装置
分析:(1)分离空气的过程中没有新物质生成,属于物理变化;
(2)过氧化氢在二氧化锰的催化作用下,分解能生成水和氧气;用排水法收集氧气时,通过观察即可判断氧气是否已经收集满;
(3)实验室中用大理石或石灰石与稀盐酸反应制取二氧化碳.
(2)过氧化氢在二氧化锰的催化作用下,分解能生成水和氧气;用排水法收集氧气时,通过观察即可判断氧气是否已经收集满;
(3)实验室中用大理石或石灰石与稀盐酸反应制取二氧化碳.
解答:解:(1)高锰酸钾受热分解、过氧化氢分解、氯酸钾受热分解、电解水等过程中都有新物质生成,属于化学变化;分离空气的过程中没有新物质生成,属于物理变化.故填:A.
(2)过氧化氢在二氧化锰的催化作用下,分解能生成水和氧气,反应的化学方程式为:2H2O2
2H2O+O2↑.
用排水法收集氧气时,如果气泡从集气瓶口外逸,说明已经收集满.故填:C.
(3)实验室用大理石或石灰石与稀盐酸反应时不需要加热,可以用B装置,二氧化碳能溶于水,密度比空气大,只能用向上排空气法收集.故填:BD.
(2)过氧化氢在二氧化锰的催化作用下,分解能生成水和氧气,反应的化学方程式为:2H2O2
| ||
用排水法收集氧气时,如果气泡从集气瓶口外逸,说明已经收集满.故填:C.
(3)实验室用大理石或石灰石与稀盐酸反应时不需要加热,可以用B装置,二氧化碳能溶于水,密度比空气大,只能用向上排空气法收集.故填:BD.
点评:本题主要考查制取氧气的方法和化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目


