题目内容
回答以下有关的问题
(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是 .钢铁属于 (填“纯净物”或“混合物”);
(2)氢气可以还原磁铁矿中的Fe3O4,请写出氢气与四氧化三铁在高温下反应的化学方程式: ;
(3)人在剧烈运动后,血液中产生较多的乳酸(化学式为C3H6O3),使肌肉酸痛,放松一段时间后,由于乳酸与吸入的氧气反应而生成二氧化碳和水,使肌肉的酸痛感消失,该反应的化学方程式是 .
漂白粉可用于饮用水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO)2],次氯酸钙可发生如下反应:Ca(ClO)2+X+H2O=CaCO3↓+2HClO,则X的化学式为 .
(1)金属元素在自然界中分布很广,地壳中含量最多的金属元素是
(2)氢气可以还原磁铁矿中的Fe3O4,请写出氢气与四氧化三铁在高温下反应的化学方程式:
(3)人在剧烈运动后,血液中产生较多的乳酸(化学式为C3H6O3),使肌肉酸痛,放松一段时间后,由于乳酸与吸入的氧气反应而生成二氧化碳和水,使肌肉的酸痛感消失,该反应的化学方程式是
漂白粉可用于饮用水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO)2],次氯酸钙可发生如下反应:Ca(ClO)2+X+H2O=CaCO3↓+2HClO,则X的化学式为
考点:地壳中元素的分布与含量,纯净物和混合物的判别,质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律,金属与金属材料
分析:(1)根据地壳中含量多的前五种元素和混合物的概念考虑;
(2)根据反应物、生成物和反应条件及质量守恒定律的两个原则,写出正确的化学方程式;
(3)根据反应物、生成物和反应条件及质量守恒定律的两个原则,写出正确的化学方程式;
(4)根据质量守恒定律可知:反应前后元素种类不变,原子个数不变.由以上依据可推出X的化学式.
(2)根据反应物、生成物和反应条件及质量守恒定律的两个原则,写出正确的化学方程式;
(3)根据反应物、生成物和反应条件及质量守恒定律的两个原则,写出正确的化学方程式;
(4)根据质量守恒定律可知:反应前后元素种类不变,原子个数不变.由以上依据可推出X的化学式.
解答:解:(1)地壳中含量多的前五种元素:氧、硅、铝、铁、钙,所以最多的金属元素是铝;钢铁中含有铁、碳等多种物质,属于混合物,故填:铝;混合物;
(2)氢气还原Fe3O4的反应物是Fe3O4和氢气,生成物是铁和水,用观察法配平,反应条件是高温,故填:4H2+Fe3O4
3Fe+4H2O.
(3)乳酸与氧气反应生成二氧化碳和水,方程式为:C3H6O3+3O2=3H2O+3CO2 ,故答案为:C3H6O3+3O2=3H2O+3CO2
(4)根据所给化学方程式可以看出:化学方程式的右边比左边多出了1个碳原子和2个氧原子;根据质量守恒定律中的元素种类不变和原子个数不变的特点,可知多出的原子全部来自1个X分子中,即X的化学式为CO2.故答案为:CO2.
(2)氢气还原Fe3O4的反应物是Fe3O4和氢气,生成物是铁和水,用观察法配平,反应条件是高温,故填:4H2+Fe3O4
| ||
(3)乳酸与氧气反应生成二氧化碳和水,方程式为:C3H6O3+3O2=3H2O+3CO2 ,故答案为:C3H6O3+3O2=3H2O+3CO2
(4)根据所给化学方程式可以看出:化学方程式的右边比左边多出了1个碳原子和2个氧原子;根据质量守恒定律中的元素种类不变和原子个数不变的特点,可知多出的原子全部来自1个X分子中,即X的化学式为CO2.故答案为:CO2.
点评:写化学方程式要注意根据题目要求,写出符合题目要求的化学方程式.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
实验室有一瓶无色气体,该气体可能是由H2、CH4、CO、CO2中的几种组成的.为了测定该瓶气体的成分,张乐进行了以下操作,根据实验现象判断下列说法正确的是( )
①将些混合气体通入盛有足量澄清的石灰水的烧杯中,杯中无明显现象;
②将气体干燥后点燃,罩在火焰上方的干燥烧杯内壁有水珠生成.
①将些混合气体通入盛有足量澄清的石灰水的烧杯中,杯中无明显现象;
②将气体干燥后点燃,罩在火焰上方的干燥烧杯内壁有水珠生成.
| A、A该混合气体中可能含有CO2 |
| B、该混合气体中一定含有H2 |
| C、该混合气体中一定含有CO |
| D、该混合气体可能是CH4和CO |
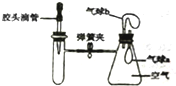 如图所示,装置气密性良好,弹簧夹处于关闭状态.挤压胶头滴管加入液体,一段时间后,打开弹簧夹,气球b不一定鼓起的是( )
如图所示,装置气密性良好,弹簧夹处于关闭状态.挤压胶头滴管加入液体,一段时间后,打开弹簧夹,气球b不一定鼓起的是( )| 试管内物质 | 胶头滴管内物质 | |
| A | 生石灰 | 水 |
| B | 镁条 | 稀盐酸 |
| C | 二氧化锰 | 过氧化氢 |
| D | 二氧化碳 | 氢氧化钠溶液 |
| A、A、 | B、B、 | C、C、 | D、D、 |
把下列物质:①浓盐酸 ②浓硫酸 ③蒸馏水 ④熟石灰 ⑤烧碱分别放置于敞口容器中,放置一段时间后,其中质量增加的是( )
| A、①②③ | B、②④⑤ |
| C、①② | D、④⑤ |
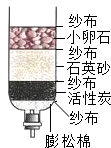 水是人类不可缺少的物质.
水是人类不可缺少的物质.