题目内容
1.请根据如表回答有关问题.(第(1)小题用序号填写)| 序号 | ① | ② | ③ | ④ |
| 物质 | 醋酸 | 高锰酸钾 | 熟石灰 | 纯碱 |
| 化学式 | KMnO4 | Ca(OH)2 |
(2)用表中的物质作为反应物,写出制取氢氧化钠的化学方程式:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
分析 (1)根据物质的名称、俗称及其化学式;根据物质的分类来分析;
(2)根据化学反应的原理结合化学方程式的写法来分析.
解答 解:(1)醋酸的化学式为CH3COOH,纯碱是碳酸钠的俗称,其化学式为Na2CO3;在四种物质中,熟石灰是氢氧化钙的俗称,是由金属离子与氢氧根离子构成的化合物,属于碱,醋酸是一种含碳元素的化合物,属于有机物;故填:CH3COOH;Na2CO3;③;①;
(2)熟石灰能与纯碱发生复分解反应生成碳酸钙沉淀和氢氧化钠;故填:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
点评 本题难度不大,主要考查同学们对常见化学用语(分子符号、化学式、离子符号等)的书写和理解能力.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
11.我国科学家用滤纸和二氧化钛(TiO2)薄膜制作出一种新型“纳米纸”,又在纳米纸上“铺”一层“萘胺”(C10H9N)染料,制成一种试纸,用于检测食品中亚硝酸盐浓度的高低.下列说法正确的是( )
| A. | 二氧化钛中含有3个原子 | |
| B. | 萘胺中C、H、N的原子个数比为10:9:1 | |
| C. | 二氧化钛和萘胺都是有机物 | |
| D. | 这种试纸是一种新型化合物 |
12.20℃时,25g水中溶解0.4g某物质即达到饱和,该物质的溶解性是( )
| A. | 难溶 | B. | 易溶 | C. | 可溶 | D. | 微溶 |
9.市场上有一种加酶洗衣粉,衣物上的汗渍、血迹及人体排放的蛋白质油渍遇到这种加酶洗衣粉都能被分解而除去.下列衣料①羊毛织品;②棉织品;③化纤布料;④蚕丝织品.其中不宜用加酶洗衣粉洗涤的是( )
| A. | ①④ | B. | ③④ | C. | ①② | D. | ②③ |
16.在通常情况下,鉴别氢气和氧气不可以利用的方法是( )
| A. | 分别用带火星的木条伸入气体中 | B. | 观察颜色、状态、闻气味 | ||
| C. | 分别用吹肥皂泡的方法 | D. | 通电电解后利用电极来判断 |
13.镍粉常用于各种高光泽装饰漆和塑料生产,也常用作催化剂.
I、【镍粉制备】:工业用电解镍新液(主要含NiSO4、NiCl2)制备碱式碳酸镍晶体 xNiCO3•yNi(OH)2•zH2O,并利用其制备镍粉的流程如下:
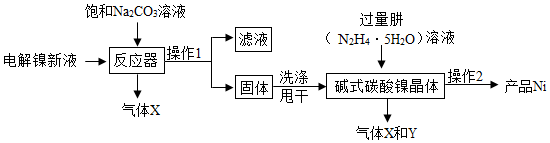
(1)反应器中一个重要反应为 3NiSO4+3Na2CO3+2H2O=NiCO3•2Ni(OH)2+3Na2SO4+2X,X的化学式为CO2.
(2)物料在反应器中反应时需要控制反应条件.分析下图,反应器中最适合的温度及pH分别为55℃、8.3.
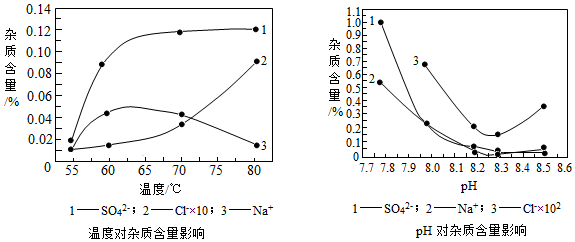
(3)生产中,pH逐渐增加,生成Ni(OH)2含量也相对增加,则生成的碱式碳酸镍晶体 中,镍的含量将升高(填“升高”、“降低”或“不变”).
Ⅱ.【测定碱式碳酸镍晶体的组成】:为测定碱式碳酸镍晶体(xNiCO3•Ni(OH)2•zH2O)组成,某小组设计了如下实验方案及装置:
【资料卡片】
1、碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O.
2、400℃左右,NiO会氧化生成Ni2O3.
3、碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O.
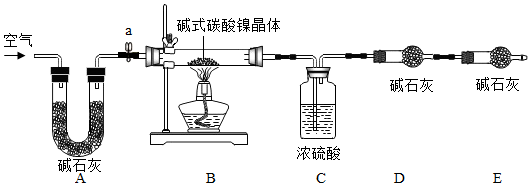
【实验步骤】:
①检查装置的气密性;②准确称取3.77gxNiCO3•yNi(OH)2•zH2O放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,称量装置C、D的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,鼓入空气;⑥准确称量装置C、D的质量;⑦根据数据进行计算(相关数据如下表).
【实验分析及数据处理】:
(4)完善实验步骤中的填空:①检查装置的气密性;⑤鼓入空气.
(5)装置E的作用是装置右侧的空气进入装置内造成干扰;
(6)计算 xNiCO3•yNi(OH)2•zH2O中x:y:z 的值1:1:4.
【实验反思】:
(7)实验结束后,称得装置B中残留固体质量为2.33g.请通过计算确定残留固体的组成及各成分的质量(精确到小数点后两位)NiO和Ni2O3混合物,其中NiO的质量为1.50g而Ni2O3的质量为0.83g.
I、【镍粉制备】:工业用电解镍新液(主要含NiSO4、NiCl2)制备碱式碳酸镍晶体 xNiCO3•yNi(OH)2•zH2O,并利用其制备镍粉的流程如下:

(1)反应器中一个重要反应为 3NiSO4+3Na2CO3+2H2O=NiCO3•2Ni(OH)2+3Na2SO4+2X,X的化学式为CO2.
(2)物料在反应器中反应时需要控制反应条件.分析下图,反应器中最适合的温度及pH分别为55℃、8.3.

(3)生产中,pH逐渐增加,生成Ni(OH)2含量也相对增加,则生成的碱式碳酸镍晶体 中,镍的含量将升高(填“升高”、“降低”或“不变”).
Ⅱ.【测定碱式碳酸镍晶体的组成】:为测定碱式碳酸镍晶体(xNiCO3•Ni(OH)2•zH2O)组成,某小组设计了如下实验方案及装置:
【资料卡片】
1、碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O.
2、400℃左右,NiO会氧化生成Ni2O3.
3、碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O.

【实验步骤】:
①检查装置的气密性;②准确称取3.77gxNiCO3•yNi(OH)2•zH2O放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,称量装置C、D的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,鼓入空气;⑥准确称量装置C、D的质量;⑦根据数据进行计算(相关数据如下表).
| 装置C/g | 装置D/g | 装置E/g | |
| 加热前 | 200.00 | 180.00 | 180.00 |
| 加热后 | 201.08 | 180.44 | 180.00 |
(4)完善实验步骤中的填空:①检查装置的气密性;⑤鼓入空气.
(5)装置E的作用是装置右侧的空气进入装置内造成干扰;
(6)计算 xNiCO3•yNi(OH)2•zH2O中x:y:z 的值1:1:4.
【实验反思】:
(7)实验结束后,称得装置B中残留固体质量为2.33g.请通过计算确定残留固体的组成及各成分的质量(精确到小数点后两位)NiO和Ni2O3混合物,其中NiO的质量为1.50g而Ni2O3的质量为0.83g.
10.将200克20%的稀硫酸加入到盛有200克20%的NaOH溶液的小烧杯中,下列说法正确的是( )
| A. | 得到的溶液质量为400克 | B. | 该反应吸收热量 | ||
| C. | 得到的溶液呈中性 | D. | 该反应不属于中和反应 |
19.在一次实验课上,浩明同学探究氢氧化钠溶液与稀硫酸能否发生反应,请你一起完成下列问题.【活动探究】浩明同学发现向氢氧化钠溶液中滴加几滴酚酞溶液,溶液办成红色,当向溶液中继续滴加稀硫酸后,红色又褪去,得到无色溶液.根据实验现象,你认为氢氧化钠溶液与稀硫酸能(填”能”或”不能”)发生反应,理由是氢氧化钠溶液呈碱性,能使酚酞变红,而红色消失说明溶液的碱性消失,也说明氢氧化钠与硫酸发生了化学反应生成了其他不显碱性的物质.
【猜想与假设】针对上述问题你还想探究的问题是反应后的溶液呈中性还是酸性;
【方案与验证】浩明同学设计如下实验继续探究:
【反思与评价】你认为小明同学的结论正确吗?理由是不正确,氢氧化钠与硫酸反应一定生成硫酸钠,硫酸钠能与氯化钡反应生成白色硫酸钡沉淀,即使硫酸没有剩余,也会产生白色沉淀
【拓展与应用】张聪认为,要证明反应后的溶液中含有硫酸应加做一个实验,请你把实验完成.
【猜想与假设】针对上述问题你还想探究的问题是反应后的溶液呈中性还是酸性;
【方案与验证】浩明同学设计如下实验继续探究:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量无色溶液于试管中,滴加氯化钡溶液 | 产生白色沉淀 | 反应后的溶液中还有硫酸剩余 |
【拓展与应用】张聪认为,要证明反应后的溶液中含有硫酸应加做一个实验,请你把实验完成.
| 实验步骤 | 实验现象 | 实验结论 |
| 反应后的溶液中还有硫酸剩余 |