题目内容
4. 我们莒县矿产资源丰富,初步探明的矿产达30多种,其中石灰石、大理石等资源尤为丰富,小华同学就从其家乡棋山镇取了石灰石样品12g放入烧杯中进行测定实验,实验中他不断地向烧杯中加入一定浓度的稀盐酸,并绘制了加入稀盐酸的质量与放出气体质量的坐标图(见图),他共加入了100g稀盐酸(石灰石中的杂质不溶于水,也不反应).
我们莒县矿产资源丰富,初步探明的矿产达30多种,其中石灰石、大理石等资源尤为丰富,小华同学就从其家乡棋山镇取了石灰石样品12g放入烧杯中进行测定实验,实验中他不断地向烧杯中加入一定浓度的稀盐酸,并绘制了加入稀盐酸的质量与放出气体质量的坐标图(见图),他共加入了100g稀盐酸(石灰石中的杂质不溶于水,也不反应).计算:
(1)该石灰石样品中碳酸钙的质量为9g.
(2)当盐酸和石灰石恰好完全反应时,所得溶液中溶质的质量分数是多少?(规范写出此问计算过程)
分析 利用碳酸钙与盐酸反应的化学方程式,根据二氧化碳的质量求出碳酸钙的质量,再根据质量分数的计算公式求出石灰石样品中碳酸钙的质量分数即可.
解答 解:(1)图象的转折点是二者恰好反应的点,此时用去稀盐酸的质量为94.86g.
该样品最多与盐酸反应生成CO23.96g.
设CaCO3质量为x,生成CaCl2质量为y.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
x y 3.96g
$\frac{100}{x}=\frac{111}{y}=\frac{44}{3.96g}$
x=9g,y=9.99g
答:该石灰石样品中碳酸钙的质量为9g;
(2)反应后氯化钙溶液的质量为:$\frac{9.99g}{9g+94.86g-3.96g}×100%$=10%;
答:恰好完全反应时,所得溶液中溶质的质量分数是10%.
点评 本题主要考查根据化学方程式的计算,难度较小.石灰石为混合物,石灰石中除了碳酸钙之外还有杂质,不能将石灰石的质量直接代入化学方程式进行计算.

练习册系列答案
相关题目
6.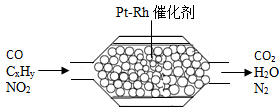 汽车尾气催化净化装置可有效处理汽车尾气带来的污染,如图是表示某汽车尾气净化器处理汽车尾气的过程,下列有关叙述不正确的是( )
汽车尾气催化净化装置可有效处理汽车尾气带来的污染,如图是表示某汽车尾气净化器处理汽车尾气的过程,下列有关叙述不正确的是( )
 汽车尾气催化净化装置可有效处理汽车尾气带来的污染,如图是表示某汽车尾气净化器处理汽车尾气的过程,下列有关叙述不正确的是( )
汽车尾气催化净化装置可有效处理汽车尾气带来的污染,如图是表示某汽车尾气净化器处理汽车尾气的过程,下列有关叙述不正确的是( )| A. | CO氧化为CO2所需氧来源于NOX | |
| B. | 汽车安装这种净化器后,能避免铅污染 | |
| C. | Pt-Rh催化剂化学反应前后质量不变 | |
| D. | 使用该净化器能减少酸雨的发生 |
19.下列各组物质的鉴别中,所选的鉴别试剂,不正确的是( )
| 待鉴别的物质 | 鉴别试剂 | |
| A | Na2CO3溶液、NaCl溶液、HCl溶液 | 石蕊溶液 |
| B | 氢氧化钠溶液和氢氧化钙溶液 | 稀盐酸 |
| C | 硬水与软水 | 肥皂水 |
| D | 硝酸铵固体与氢氧化钠固体 | 水 |
| A. | A | B. | B | C. | C | D. | D |
9.下列化学方程式符合事实且书写正确的是( )
| A. | 2NaOH+SO2→Na2SO4+H2O | B. | 2Fe+6HCl→2FeCl3+3H2↑ | ||
| C. | K2CO3+2HCl→2KCl+H2CO3 | D. | Fe2O3+3H2SO4→Fe2(SO4)3+3H2O |
16.下列图示实验操作中,错误的是( )
| A. |  液体的倾倒 | B. |  检验氧气是否集满 | ||
| C. |  给液体加热 | D. |  称取一定质量的NaOH |
14.下列了属于纯净物的是( )
| A. | 大理石 | B. | 食醋 | C. | 加碘食盐 | D. | 五氧化二磷 |