题目内容
13.根据如图所示的实验来回答下列问题.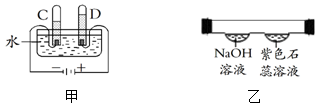
(1)如图甲所示的是电解水的实验装置.电解水的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$O2↑+2H2↑,其中C试管中的气体是氢气.
(2)在如图乙所示的实验中,紫色石蕊溶液变为蓝色,这个实验证明了分子在不断的运动的和氢氧化钠溶液呈碱性.
分析 (1)根据电解水生成氢气和氧气,结合电解水的实验结论(正氧负氢、氢二氧一),进行分析解答.
(2)根据题意,紫色石蕊溶液变为蓝色,而两者没有接触,进行分析解答.
解答 解:(1)电解水生成氢气和氧气,反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$O2↑+2H2↑;电解水时,与电源负极相连的试管内的气体体积多,是氢气,与电源正极相连的试管内产生的气体体积少,是氧气,C试管与电源的负极相连,气体是氢气.
(2)由题意,如图乙所示的实验中,紫色石蕊溶液变为蓝色,而两者没有接触,说明分子在不断的运动的;紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝,紫色石蕊溶液变为蓝色,说明氢氧化钠溶液呈碱性.
故答案为:(1)2H2O$\frac{\underline{\;通电\;}}{\;}$O2↑+2H2↑;氢气;(2)分子在不断的运动的,氢氧化钠溶液呈碱性
点评 本题难度不大,掌握碱的化学性质、电解水的实验结论(正氧负氢、氢二氧一)等是正确解答本题的关键.

练习册系列答案
相关题目
1.下列图象能正确反映其对应关系的是( )


| A. | 用一氧化碳还原一定质量的氧化铁 | |
| B. | 在两份等质量、等溶质质量分数的过氧化氢溶液中,一份加催化剂,一份不加催化剂 | |
| C. | 通电使水分解 | |
| D. | 向盛有等质量、等溶质质量分数的稀硫酸的两支试管中,分别加入过量的镁和铝 |
4.下列说法不正确的是 ( )
| A. | 分子、原子、离子都能直接构成物质 | |
| B. | 熟石灰可以改良酸性土壤,但不能和铵态氮肥混合使用 | |
| C. | 塑料大量使用,会造成“白色污染” | |
| D. | 木炭燃烧的剧烈程度由它的着火点决定,而与氧气的浓度无关 |
8.逻辑推理是化学学习中常用的思维方法.以下推理正确的是( )
| A. | 中和反应有盐和水生成,但有盐和水的反应一定都属于中和反应 | |
| B. | 合金是在某种金属中加热熔合其他金属或非金属形成的,所有合金一定属于混合物 | |
| C. | 氧化物中含有氧元素,所以含有氧元素的化合物一定是氧化物 | |
| D. | 化学反应通常伴有能量变化,所以凡是伴有能量变化的一定是化学变化 |
18.化学在能源利用、环境保护等方面起着重要作用.下列有关做法不正确的是( )
| A. | 将地沟油转化为航空油,变废为宝 | |
| B. | 使用新型的可降解塑料,减少白色污染 | |
| C. | 改进汽车尾气净化技术,减少有害气体排放 | |
| D. | 加高化工厂的烟囱排放废气,防止形成酸雨 |
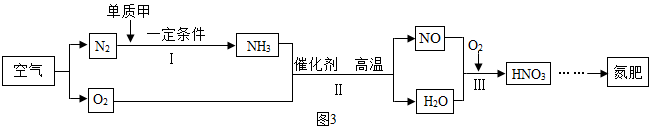
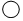 ”表示氮原子,“
”表示氮原子,“ ”表示氧原子.
”表示氧原子. ”可表示的微粒是氮分子(填名称).
”可表示的微粒是氮分子(填名称).