题目内容
下列实验操作中不能达到实验目的的是
选项 | 物质 | 目的 | 主要实验操作 |
A | NH4NO3和NaCl | 鉴别 | 分别加水溶解,测温度变化 |
B | CaCl2溶液中混有盐酸 | 除杂 | 加入过量的CaCO3粉末,过滤 |
C | CH4中是否含有H2 | 检验 | 点燃,罩一干冷烧杯,观察燃烧产物 |
D | KCl与MnO2固体混合物 | 分离 | 加水充分溶解后过滤、洗涤、烘干、蒸发 |
A. A B. B C. C D. D
C 【解析】A、NH4NO3溶于水,吸收大量的热,温度明显降低,NaCl溶于水温度变化不明显,正确;B、CaCO3 + 2HCl== CaCl2 + H2O + CO2↑,加入过量CaCO3粉末,将盐酸完全除去,过滤,滤出固体物质,滤液是CaCl2溶液,正确;C、CH4和H2燃烧时都生成水,干冷的烧杯内壁都有水雾出现,错误;D、KCl易溶于水,MnO2难溶于水,将KCl与MnO2固体混合物加...
练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目


 Fe(OH)2
Fe(OH)2 Fe(OH)3
Fe(OH)3 Fe2O3•xH2O
Fe2O3•xH2O
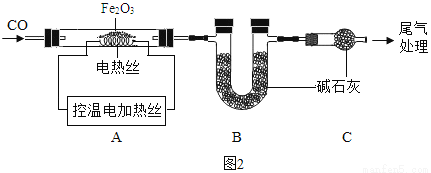
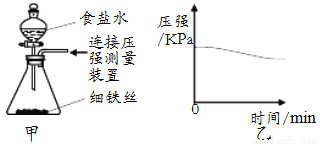
 Fe
Fe FeCl3
FeCl3 H2
H2  H2O
H2O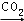 CaCO3
CaCO3  CO2
CO2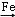 Cu
Cu 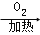 CuO
CuO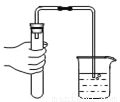 如图:检查气密性
如图:检查气密性 如图:制取
如图:制取 如图:收集
如图:收集 如图:验满
如图:验满