题目内容
18.在①碳循环②氧循环③水的天然循环三种循环过程中所发生的变化一定不需要原子重新组合就能实现的是( )| A. | ①② | B. | ②③ | C. | ①③ | D. | ③ |
分析 根据已有的知识进行分析解答,原子重新组合则是发生的化学变化,据此解答.
解答 解:①碳循环的过程是化学变化,一定需要原子重新组合,②氧循环是化学变化,一定需要原子的重新组合,③水的天然循环是物理变化,一定不需要原子的重新组合,故选D.
点评 本题考查的是化学反应的实质的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
9.推理是科学课学习中常用的思维方法.下列推理中正确的是( )
| A. | Na2CO3俗称纯碱,它的水溶液呈碱性,属于碱类 | |
| B. | 氧化物必定含有氧元素,则含氧元素的化合物必属于氧化物 | |
| C. | 同种元素可组成不同的单质,则由同种元素组成的物质也可能是混合物 | |
| D. | 盐是由金属离子和酸根离子组成的,NH4NO3中没有金属离子,不属于盐 |
13.“NaC1+CO2+NH3+H2O=NaHCO3+NH4Cl”是氨碱法制纯碱中的重要反应.下列叙述正确的是( )
| A. | 该条件下NaHCO3的溶解度比NH4C1的大 | |
| B. | 析出晶体后的溶液为NaHCO3的不饱和溶液 | |
| C. | 在加压的条件下向饱和氨盐水中通二氧化碳,能加速NaHCO3的生成 | |
| D. | 析出晶体后剩余溶液中只有一种溶质 |
3.KCl与KNO3在不同温度的溶解度数据如表.则下列说法正确的是( )
| 温度/℃ | 10 | 20 | 30 | 40 | 50 |
| KCl | 30g | 33g | 35g | 38g | 41g |
| KNO3 | 21g | 31g | 45g | 65g | 88g |
| A. | KNO3比KCl的溶解度大 | |
| B. | 两物质都属于可溶物质 | |
| C. | 在30℃时,5gKNO3加入到10g水中可得到33.3%的KNO3溶液 | |
| D. | 在50℃时,两物质各10g分别加入20g水中,充分溶解,只有KCl中有固体剩余 |
8.烧杯中装有100克硫酸和硫酸铜的混合溶液,向该溶液中加入10%的NaOH溶液,得到沉淀的质量记录如下:
(1)加入NaOH溶液159.8克时,得到沉淀的质量不再变化.
(2)该混合溶液中CuSO4的质量为16.0克.
(3)原混合溶液中硫酸铜的质量分数?
(2、3问要求写计算过程,结果精确到小数点后一位小数)
| 加入NaOH溶液的质量/g | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
| 生产沉淀的总质量/g | 0.0 | 2.5 | 8.6 | 9.8 | 9.8 |
(2)该混合溶液中CuSO4的质量为16.0克.
(3)原混合溶液中硫酸铜的质量分数?
(2、3问要求写计算过程,结果精确到小数点后一位小数)
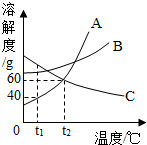 如图是A、B、C三种物质的溶解度曲线.请回答:
如图是A、B、C三种物质的溶解度曲线.请回答: