题目内容
9.表为元素周期表中某一周期元素的原子结构示意图.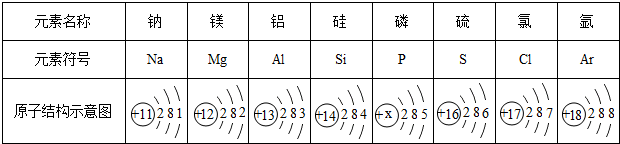
请回答下列问题:
(1)表中磷原子的核电荷数x=15.
(2)表中具有相对稳定结构的元素是Ar(氩).
(3)镁元素与氯元素形成的化合物的化学式为MgCl2.
(4)上述元素在周期表中处于同一周期的原因是电子层数相同.
(5)在化学反应中,每个铝原子失去3个电子形成铝离子.
(6)硫与氧气反应的化学方程式是:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;设N个氧气分子的质量为32g,则64g氧气与足量硫粉完全反应生成的二氧化硫分子数为2N.
分析 (1)根据原子中质子数=核外电子数,进行分析解答.
(2)最外层具有8个电子的原子具有相对稳定结构.
(3)镁元素显+3价,氯元素显-1价,写出其化学式即可.
(4)根据元素周期数与电子层数的关系进行分析解答.
(5)最外层电子数<4,则一般为金属元素,在化学反应中易失去电子,据此进行分析解答;
(6)硫与氧气反应生成二氧化硫,根据反应方程式可计算出生成二氧化硫的物质的量,并计算出分子数.
解答 解:(1)原子中质子数=核外电子数,则磷原子的核电荷数x=2+8+5=15.故填:15;
(2)最外层具有8个电子的原子具有相对稳定结构,表中具有相对稳定结构的元素氩元素.故填:Ar(氩);
(3)镁元素显+3价,氯元素显-1价,其化学式为:MgCl2.故填:MgCl2;
(4)由元素周期表中某一周期元素的原子结构示意图可以看出,处于同一周期的原子,核外电子层数相同.故填:电子层数相同;
(5)铝原子的最外层电子数为3,在化学反应中,每个铝原子失去3个电子形成铝离子;故填:3;
(6)硫与氧气反应生成二氧化硫,反应的方程式为S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;根据反应方程式可知,每个氧分子反应生成1个二氧化硫分子,设N个氧气分子的质量为32g,64g氧气应为2N,与足量硫粉完全反应生成的二氧化硫分子数为2N,故答案为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2;2.
点评 本题难度不大,考查学生对原子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是正确解题的关键.

练习册系列答案
相关题目
20.下列物质的鉴别方法,错误的是( )
| A. | 铁丝和铜丝--看颜色 | B. | 酒精和蒸馏水--闻气味 | ||
| C. | 氧气和空气--带火星的木条 | D. | 氮气和二氧化碳--燃着的木条 |
17.下列变化中,肯定发生了化学变化的是( )
| A. | 干冰升华 | B. | 石油分馏 | C. | 粗盐潮解 | D. | 高梁酿酒 |
4.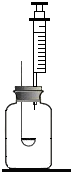 在做测定空气中氧气含量的实验中,小亮同学设计如图所示的装置(注射器中装有水,注射器活塞能自由移动),对此装置评价错误的是( )
在做测定空气中氧气含量的实验中,小亮同学设计如图所示的装置(注射器中装有水,注射器活塞能自由移动),对此装置评价错误的是( )
 在做测定空气中氧气含量的实验中,小亮同学设计如图所示的装置(注射器中装有水,注射器活塞能自由移动),对此装置评价错误的是( )
在做测定空气中氧气含量的实验中,小亮同学设计如图所示的装置(注射器中装有水,注射器活塞能自由移动),对此装置评价错误的是( )| A. | 该装置能使测量空气中氧气含量更精确 | |
| B. | 此装置可以直接测出瓶中原有的氧气质量 | |
| C. | 在探究中可以领悟科学研究的严密性和趣味性 | |
| D. | 此装置不使用导管,所以避免了反应后导管中的空气进入瓶中引起误差,又避免了导管中留有一定量的水引起误差 |