题目内容
5.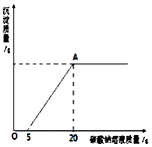 为了探究石灰石与稀盐酸反应制备二氧化碳后的废液中的溶质成分,将废液过滤,取滤液20g于烧杯中,在不断振荡的条件下,向其中滴加质量分数为10.6%的碳酸钠溶液直至过量,有关的变化如图所示:根据题中有关信息和图象分析回答下列问题
为了探究石灰石与稀盐酸反应制备二氧化碳后的废液中的溶质成分,将废液过滤,取滤液20g于烧杯中,在不断振荡的条件下,向其中滴加质量分数为10.6%的碳酸钠溶液直至过量,有关的变化如图所示:根据题中有关信息和图象分析回答下列问题(1)原废液中的溶质成分有HCl、CaCl2(用化学式回答)
(2)A点处溶液中溶质的质量是多少克?(通过计算回答)
分析 碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,和氯化钙反应生成白色沉淀碳酸钙和氯化钠;
根据碳酸钠溶液的质量和溶质质量分数可以计算沉淀碳酸钙的质量.
解答 解:(1)由图中信息可知,加入5g碳酸钠溶液时才开始产生沉淀,说明滤液中含有稀盐酸,因此原废液中的溶质成分有HCl、CaCl2.
故填:HCl、CaCl2.
(2)设反应产生的沉淀的质量为x,
和氯化钙反应的碳酸钠溶液质量为:20g-5g=15g,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 100
15g×10.6% x
$\frac{106}{100}$=$\frac{15g×10.6%}{x}$
x=1.5g,
答:A点处所得沉淀的质量是1.5g.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
15.现有100g溶质质量分数为10%的食盐溶液,若使溶液的溶质质量分数增加一倍,下列操作中正确的是( )
| A. | 加入10g食盐 | |
| B. | 加入50g水 | |
| C. | 加入100g溶质质量分数10%的食盐溶液 | |
| D. | 蒸发掉50g水 |
20.下列各组物质的溶液混合后,最终不一定有沉淀生成的是( )
| A. | 氢氧化钡 硫酸 盐酸 | B. | 氯化铜 氢氧化钠 盐酸 | ||
| C. | 氯化钡 碳酸钠 硝酸钾 | D. | 硝酸银 盐酸 碳酸钠 |
5.下列曲线图能正确表达相应反应或过程的是( )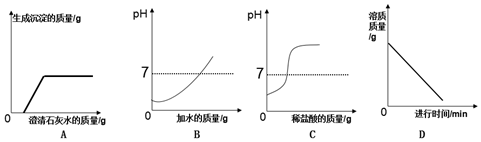

| A. | 一个烧杯中盛有稀盐酸和氯化镁溶液,滴加澄清石灰水 | |
| B. | 将 pH=1 的溶液加水稀释 | |
| C. | 向一定质量的 NaOH 溶液中滴入稀盐酸 | |
| D. | 向澄清石灰水中加入一定量的生石灰 |
10.在化肥中硝酸钾属于( )
| A. | 钾肥 | B. | 氮肥 | C. | 磷肥 | D. | 复合肥 |
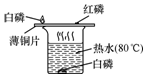 某同学为探究可燃物燃烧的条件,他查阅资料得知:白磷的着火点为40℃,红磷的着火点为240℃,它们在空气中燃烧都会产生白烟--五氧化二磷,五氧化二磷易溶于水,并能与水反应.
某同学为探究可燃物燃烧的条件,他查阅资料得知:白磷的着火点为40℃,红磷的着火点为240℃,它们在空气中燃烧都会产生白烟--五氧化二磷,五氧化二磷易溶于水,并能与水反应.