题目内容
13.K+的离子结构示意图如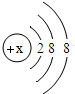 :
:(1)x的值是19.
(2)下列微粒示意图所表示的元素的化学性质与K的化学性质相似的是B(填字母,下同),属于离子的是D.
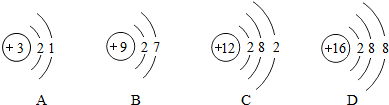
(3)实验室常温下制氧气的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
分析 (1)K+是钾原子失去1个电子得到的,据此进行分析解答.
(2)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;据此进行分析解答.
(3)实验室常温下制氧气采用的是分解过氧化氢的方法,过氧化氢在二氧化锰的催化作用下生成水和氧气,写出反应的化学方程式即可.
解答 解:(1)K+是钾原子失去1个电子得到的,则x=2+8+8+1=19.
(2)决定元素化学性质的是最外层电子数,原子的最外层电子数相同,具有相似的化学性质;钾原子的最外层电子数为7,则与其化学性质相似的粒子结构示意图中最外层电子数也应为7,B符合要求.
D质子数=16,核外电子数=18,质子数<核外电子数,为阴离子.
(3)实验室常温下制氧气采用的是分解过氧化氢的方法,过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
故答案为:(1)19;(2)B;D;(3)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.

练习册系列答案
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
4.下列是除去粗盐中难溶性杂质的各步操作,错误的是( )
| A. | 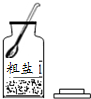 | B. |  | C. |  | D. |  |
1.下列各组物质在水溶液中能大量共存,而且加入无色酚酞溶液后显红色的是( )
| A. | NaOH NaCl CuSO4 HCl | B. | KNO3 Na2SO4 NaOH KCl | ||
| C. | KCl Ba(NO3)2 HCl CaCl2 | D. | Na2CO3 Ba(OH)2 KNO3 Na2SO4 |
8.亚硝酸钠(NaNO2)是一种污染物,有毒.金属加工废切削液中常含此物质,人们常用以下方法来处理:
第一步:NaNO2+NH4Cl=NH4NO2+NaCl
第二步:NH4NO2$\frac{\underline{\;\;△\;\;}}{\;}$X↑+2H2O.
X的化学式为( )
第一步:NaNO2+NH4Cl=NH4NO2+NaCl
第二步:NH4NO2$\frac{\underline{\;\;△\;\;}}{\;}$X↑+2H2O.
X的化学式为( )
| A. | N2O | B. | N2 | C. | H2 | D. | NO |
5.化学时刻影响着我们的生活,他在工农业生产和日常生活中起到了非常重要的作用,下列说法正确的是( )
| A. | 铁元素是人体必需的常量元素,主要存在血液中 | |
| B. | 木炭燃烧的剧烈程度由它的着火点决定,而与氧气的浓度无关 | |
| C. | 塑料都有热塑性,可以反复加工,多次使用,不会造成“白色污染” | |
| D. | 熟石灰可以改良酸性土壤,但不能和硫酸铵混合使用 |
2.新型清洁能源的使用一直是人类梦寐以求的愿望,下列能源不会对环境造成污染,且具有良好发展前景的是( )
| A. | 煤 | B. | 天然气 | C. | 氢气 | D. | 柴油 |
3.根据表提供的信息,下列判断正确的是( )
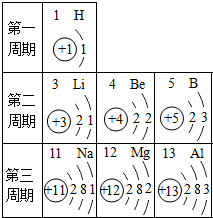

| A. | 元素所在的周期数等于其原子的电子层数 | |
| B. | 钠离子核外有三个电子层 | |
| C. | 在化学变化中镁元素容易失去最外层2个电子形成镁离子,其离子符号是Mg+2 | |
| D. | 第二、三周期元素的原子从左至右最外层电子数逐渐增多 |