题目内容
12.如图是与水有关的四个实验.请回答下列问题: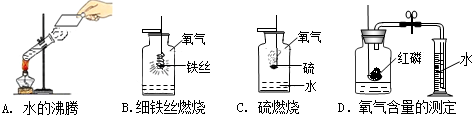
(1)A实验中,玻璃片上观察到的现象是玻璃片上有液滴出现;
(2)B实验中水的作用是防止生成物熔化溅落炸裂瓶底,发生反应的文字表达式为铁+氧气$\stackrel{点燃}{→}$四氧化三铁;
(3)C实验中不能用细砂代替水的原因是细砂不能吸收硫燃烧生成的二氧化硫气体;
(4)D实验结束后,可以通过量筒中水的体积变化测出瓶内氧气的体积.
分析 (1)根据水遇冷的现象分析回答;
(2)根据细铁丝在氧气中燃烧实验中集气瓶中水的作用和反应原理分析解答;
(3)根据水的作用是吸收生成的二氧化硫分析解答;
(4)根据实验的原理分析水倒吸入集气瓶分析解答.
解答 解:(1)水蒸气遇冷在玻璃片上凝结,故填:玻璃片上有液滴出现;
(2)集气瓶中的水是为了防止生成物熔化溅落炸裂瓶底,发生反应时铁和氧气反应生成四氧化三铁,表达式为:铁+氧气$\stackrel{点燃}{→}$四氧化三铁.故填:防止生成物熔化溅落炸裂瓶底;铁+氧气$\stackrel{点燃}{→}$四氧化三铁;
(3)C实验中水的作用是吸收硫燃烧生成的二氧化硫,如换成细砂则起不到吸收二氧化硫的作用,故填:细砂不能吸收硫燃烧生成的二氧化硫气体;
(4)D实验中集气瓶中氧气被消耗压强变小,实验后量筒中的水会进入集气瓶,根据水体积的减少,即可测出空气中氧气的含量.故填:体积.
点评 此题是氧气的化学性质、空气的组成测定等实验的综合题,解答的关键是掌握这些实验的实验原理和注意事项,属于基础考查.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
20.下列不属于化学研究对象的是( )
| A. | 空气的组成 | B. | 潮汐现象 | C. | 氧气的性质 | D. | 水分子的构成 |
7. 同学们观察了如图所示的实验后,通过认真思考和积极讨论,得出了如下结论,你认为其中不合理的是( )
同学们观察了如图所示的实验后,通过认真思考和积极讨论,得出了如下结论,你认为其中不合理的是( )
 同学们观察了如图所示的实验后,通过认真思考和积极讨论,得出了如下结论,你认为其中不合理的是( )
同学们观察了如图所示的实验后,通过认真思考和积极讨论,得出了如下结论,你认为其中不合理的是( )| A. | 空气中含有能支持红磷燃烧的物质 | |
| B. | 红磷燃烧时产生白烟,说明生成了固体小颗粒 | |
| C. | 红磷燃烧后,钟罩内的物质都不溶于水 | |
| D. | 这个实验证明了氧气占空气总体积的$\frac{1}{5}$ |
17.请结合如图回答问题:
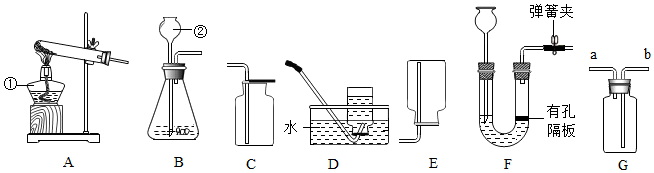
(1)写出标号①②的仪器名称:①酒精灯,②长颈漏斗.
(2)实验室用一种紫黑色固体和装置A、D制取O2,该反应的符号表达式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.图A装置中存在的一个不足之处是试管口没有放一团棉花.
(3)实验室制取CO2可选择发生装置B和收集装置C(填序号),该反应的符号表达式为CaCO3+2HCl=CaCl2+H2O+CO2↑.装置F相较于装置B,优点是便于控制反应的发生和停止.
(4)图G是某学生设计的一种有洗气、检验、贮气等用途的装置.
①当用排空气法收集二氧化碳时,瓶内没有水,气体从b(填“a”或“b”)处导管通入;
②当用排水法收集氧气时,瓶内装满水,在b(填“a”或“b”)处导管连接一根长导管,并通入量筒(填仪器名称)中,可测得收集到氧气的体积.
③当用此装置检验CO2时,瓶内装入澄清石灰水(填试剂名称),气体从b(填“a”或“b”)处通入,反应的符号表达式为Ca(OH)2+CO2=CaCO3↓+H2O.
(5)某同学在实验时,发现“不慎碰倒装满氧气的集气瓶,迅速扶起后,瓶中剩余的氧气仍能使带火星的木条复燃”;对此该同学就氧气浓度为多少时能使带火星的木条复燃设计进行了如下实验:
取5只集气瓶,编一号为①、②、③、④、⑤,分别装入其总容积10%、20%、30%、
40%、50%的水,用排水法收集氧气,恰好把5只集气瓶中的水排去,将带火星的木条依次插入①~⑤号瓶中,记录实验现象.
该同学在前一组实验的基础上又做了第二组和第三组实验,三组实验的数据和现象见表:
请根据实验问答下列问题:
①用图1方案进行第一组的⑤号集气瓶实验,其中最合理的是a(填字母),判断气体己集满的方法是液面下降至瓶口,有大气泡向瓶口逸出.
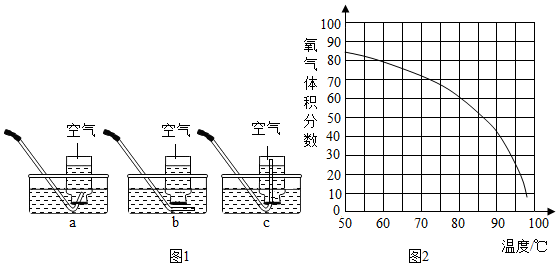
②由实验数据可知:收集的氧气占容积的体积分数最低为35%时,可使带火星的木条复燃,这时集气瓶中氧气的体积分数是48%(计算结果保留整数).
③若改用加热双氧水制氧气,则反应的符号表达式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;此时用带火星的木条直接检验产生的氧气,往往难以复燃,这是因为在加热生成氧气的同时产生大量水蒸汽,此时混合气体中氧气的体积分数随温度变化的曲线如图2所示,若只考虑氧气的体积分数对实验结果的影响,欲使带火早的木条复燃,应将双氧水的最高温度控制在87℃.

(1)写出标号①②的仪器名称:①酒精灯,②长颈漏斗.
(2)实验室用一种紫黑色固体和装置A、D制取O2,该反应的符号表达式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.图A装置中存在的一个不足之处是试管口没有放一团棉花.
(3)实验室制取CO2可选择发生装置B和收集装置C(填序号),该反应的符号表达式为CaCO3+2HCl=CaCl2+H2O+CO2↑.装置F相较于装置B,优点是便于控制反应的发生和停止.
(4)图G是某学生设计的一种有洗气、检验、贮气等用途的装置.
①当用排空气法收集二氧化碳时,瓶内没有水,气体从b(填“a”或“b”)处导管通入;
②当用排水法收集氧气时,瓶内装满水,在b(填“a”或“b”)处导管连接一根长导管,并通入量筒(填仪器名称)中,可测得收集到氧气的体积.
③当用此装置检验CO2时,瓶内装入澄清石灰水(填试剂名称),气体从b(填“a”或“b”)处通入,反应的符号表达式为Ca(OH)2+CO2=CaCO3↓+H2O.
(5)某同学在实验时,发现“不慎碰倒装满氧气的集气瓶,迅速扶起后,瓶中剩余的氧气仍能使带火星的木条复燃”;对此该同学就氧气浓度为多少时能使带火星的木条复燃设计进行了如下实验:
取5只集气瓶,编一号为①、②、③、④、⑤,分别装入其总容积10%、20%、30%、
40%、50%的水,用排水法收集氧气,恰好把5只集气瓶中的水排去,将带火星的木条依次插入①~⑤号瓶中,记录实验现象.
该同学在前一组实验的基础上又做了第二组和第三组实验,三组实验的数据和现象见表:
| 第一组 | 第二组 | 第三组 | |||||||||
| 集气瓶号 | ① | ② | ③ | ④ | ⑤ | ① | ② | ③ | ④ | ⑤ | ① |
| 收集的氧气占容积的体积分数(%) | 10 | 20 | 30 | 40 | 50 | 31 | 33 | 35 | 37 | 39 | 34 |
| 带火星的木条的状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 | 很亮 | 很亮 | 复燃 | 复燃 | 复燃 | 很亮 |
①用图1方案进行第一组的⑤号集气瓶实验,其中最合理的是a(填字母),判断气体己集满的方法是液面下降至瓶口,有大气泡向瓶口逸出.

②由实验数据可知:收集的氧气占容积的体积分数最低为35%时,可使带火星的木条复燃,这时集气瓶中氧气的体积分数是48%(计算结果保留整数).
③若改用加热双氧水制氧气,则反应的符号表达式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;此时用带火星的木条直接检验产生的氧气,往往难以复燃,这是因为在加热生成氧气的同时产生大量水蒸汽,此时混合气体中氧气的体积分数随温度变化的曲线如图2所示,若只考虑氧气的体积分数对实验结果的影响,欲使带火早的木条复燃,应将双氧水的最高温度控制在87℃.
4.下列为了达到实验目的而进行的实验操作,其中正确的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 洗涤内壁沾有油脂的试管 | 用大量的水冲洗 |
| B | 检验集气瓶中O2是否集满 | 将燃着的木条伸入集气瓶 |
| C | 检测CO中是否混有CO2 | 将气体通入澄清石灰水 |
| D | 除去KCl粉末中混有的K2SO4 | 加水溶解,过滤,蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
2.如图所示的装置,其中可以收集氧气的是( )
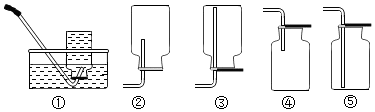

| A. | ①和 ②② | B. | ②和 ③ | C. | ①和 ④ | D. | ①和 ⑤ |
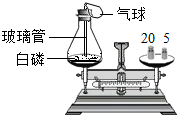 为了研究质量守恒定律,设计了如图“白磷燃烧前后质量测定”的实验,请分析有关问题:
为了研究质量守恒定律,设计了如图“白磷燃烧前后质量测定”的实验,请分析有关问题: