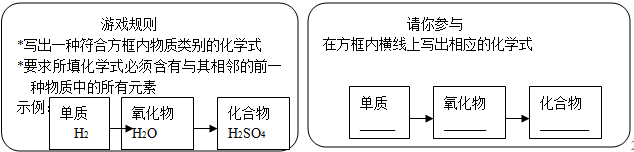
题目内容
5.根据质量守恒定律推测,反应4X+502=4NO+6H20,X的化学式为( )| A. | NH3 | B. | N2 | C. | H2 | D. | H20 |
分析 由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物X的化学式.
解答 解:根据反应的化学方程式4X+502=4NO+6H20和质量守恒定律:反应前后,原子种类、数目均不变,可知:反应物中氧原子个数为10,而反应后的生成物中氮、氢、氧原子个数分别为4、12、10,根据反应前后原子种类、数目不变,4X含有4个氮原子和12个氢原子,则每个X分子1个氮原子和3个氢原子构成,则物质X的化学式为NH3.
故选:A.
点评 本题难度不大,利用化学反应前后原子守恒来确定物质的化学式是正确解答此类题的关键.

练习册系列答案
相关题目
15.下列有关实验现象的描述,正确的是( )
| A. | 白磷在空气中燃烧,产生大量白烟 | |
| B. | 镁带在空气中燃烧,发出耀眼的强光,生成白色的氧化镁 | |
| C. | 铁丝在空气中剧烈燃烧火星四射,生成黑色固体 | |
| D. | 木炭在氧气中燃烧发出明亮的火焰,放出热量 |
16.下列实验操作正确的是( )
| A. |  液体加热 | B. | 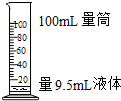 | C. | 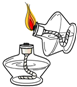 点燃酒精灯 | D. | 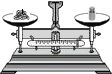 称量10.05g固体 称量10.05g固体 |
14.碳元素是日常生活中接触非常多的一种元素,碳元素也形成了各种单质、化合物及混合物,让我们和大家一起走进他们的世界

(1)根据表1提供的信息,填写有关含碳物质的对应特性.
(2)液态二氧化碳灭火器可用于扑救档案资料室发生的火灾,下列说法正确的有AB(填标号).
A.液态二氧化碳气化后不会污染档案资料
B.二氧化碳可覆盖在燃烧物表面,隔绝空气
C.液态二氧化碳气化时吸热,降低了可燃物的着火点
(3)小凤又在一本参考书上发现,镁也能在二氧化碳中燃烧!于是她做了这个实验(如图1),将镁条点燃后迅速伸入盛有二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种白色粉末和一种黑色粉末.根据上述现象,写出该反应的化学方程式:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
这个实验还引发了我们对过去某些知识的反思,从而有了新的发现,新的发现是ABC(填序号)
A.在一定的条件下,二氧化碳也能支持燃烧;
B.活泼金属着火时不能用二氧化碳灭火;
C.燃烧不一定需要有氧气.
(4)“神州十号”飞船的成功发射是我国航天事业的又一里程碑.金属过氧化物等可作宇宙飞船或潜水艇中的氧气再生剂,如:淡黄色的过氧化钠固体(Na2O2)在常温下能与人呼出的二氧化碳反应生成白色碳酸钠固体和氧气,为了验证该反应中氧气的产生,某兴趣小组的同学设计了如图2所示的实验.
①过氧化钠固体(Na2O2)与二氧化碳反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2.
②A装置中所发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;
③表明二氧化碳没有被过氧化钠完全吸收的现象是C装置处的澄清石灰水变浑浊.
(5)小明欲探究过氧化钠吸收和释放的气体之间体积关系以及反应的热效应,设计实验如下,请回答下列相关问题:
①检查装置气密性的方法:用其中一只注射器中抽取一定体积空气,如图3连好装置,缓缓推动,若能观察
到推动A注射器的活塞,则B中活塞向右移动,说明气密性良好.
②向U形管内盛装过量的Na2O2药品,注射器中为二氧化碳气体,连接好装置.药品为什么需过量确保二氧化碳完全反应,得到纯净的氧气.
③缓缓推动注射器A活塞,片刻,可以观察到温度计液柱明显上升,说明反应放热(填“吸热”或“放热”)同时还可以观察到固体粉末发生变化的现象是黄色变白;
④小明查阅资料得知:相同的条件下,相同体积的气体具有相等的分子数,则待A注射器中二氧化碳气体反应完全后,装置恢复至常温,B注射器中活塞应停留在50mL处.(不考虑实验带来的误差)
⑤小红同学通过查阅资料了解到Na2O2还能与水反应,方程式为:2Na2O2+2H2O═4NaOH+O2↑于是她根据这一原理设计了另一种测定Na2O2的纯度的方法:①称取20g样品于一只质量为45g的锥形中;②一次性加入20mL蒸馏水后将锥形瓶放置在电子天平上(如图4),观察显示数字的变化,并记录(数据见表2);③进行计算.
i从上表数据判断,240秒时,已经反应完全;
ii请你帮小红同学计算此样品中Na2O2的纯度,并写出过程.

(1)根据表1提供的信息,填写有关含碳物质的对应特性.
| 物质用途 | 石墨作电极 | 活性炭净水 |
| 对应特征 | 导电性 | 吸附性 |
A.液态二氧化碳气化后不会污染档案资料
B.二氧化碳可覆盖在燃烧物表面,隔绝空气
C.液态二氧化碳气化时吸热,降低了可燃物的着火点
(3)小凤又在一本参考书上发现,镁也能在二氧化碳中燃烧!于是她做了这个实验(如图1),将镁条点燃后迅速伸入盛有二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种白色粉末和一种黑色粉末.根据上述现象,写出该反应的化学方程式:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;
这个实验还引发了我们对过去某些知识的反思,从而有了新的发现,新的发现是ABC(填序号)
A.在一定的条件下,二氧化碳也能支持燃烧;
B.活泼金属着火时不能用二氧化碳灭火;
C.燃烧不一定需要有氧气.
(4)“神州十号”飞船的成功发射是我国航天事业的又一里程碑.金属过氧化物等可作宇宙飞船或潜水艇中的氧气再生剂,如:淡黄色的过氧化钠固体(Na2O2)在常温下能与人呼出的二氧化碳反应生成白色碳酸钠固体和氧气,为了验证该反应中氧气的产生,某兴趣小组的同学设计了如图2所示的实验.
①过氧化钠固体(Na2O2)与二氧化碳反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2.
②A装置中所发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑;
③表明二氧化碳没有被过氧化钠完全吸收的现象是C装置处的澄清石灰水变浑浊.
(5)小明欲探究过氧化钠吸收和释放的气体之间体积关系以及反应的热效应,设计实验如下,请回答下列相关问题:
①检查装置气密性的方法:用其中一只注射器中抽取一定体积空气,如图3连好装置,缓缓推动,若能观察
到推动A注射器的活塞,则B中活塞向右移动,说明气密性良好.
②向U形管内盛装过量的Na2O2药品,注射器中为二氧化碳气体,连接好装置.药品为什么需过量确保二氧化碳完全反应,得到纯净的氧气.
③缓缓推动注射器A活塞,片刻,可以观察到温度计液柱明显上升,说明反应放热(填“吸热”或“放热”)同时还可以观察到固体粉末发生变化的现象是黄色变白;
④小明查阅资料得知:相同的条件下,相同体积的气体具有相等的分子数,则待A注射器中二氧化碳气体反应完全后,装置恢复至常温,B注射器中活塞应停留在50mL处.(不考虑实验带来的误差)
⑤小红同学通过查阅资料了解到Na2O2还能与水反应,方程式为:2Na2O2+2H2O═4NaOH+O2↑于是她根据这一原理设计了另一种测定Na2O2的纯度的方法:①称取20g样品于一只质量为45g的锥形中;②一次性加入20mL蒸馏水后将锥形瓶放置在电子天平上(如图4),观察显示数字的变化,并记录(数据见表2);③进行计算.
| 时间/s | 60 | 120 | 180 | 240 | 300 |
| 天平示数/g | 83.82 | 82.43 | 82.15 | 81.80 | 81.80 |
ii请你帮小红同学计算此样品中Na2O2的纯度,并写出过程.
15.某种含硫酸亚铁的药物可用于治疗缺铁性贫血.某贫血患者每天需服用这种含铁元素10%的药物224mg,则每天他服用的这种药物中含硫酸亚铁(FeSO4)的质量是(该药物中其它成分不含铁元素)( )
| A. | 30.4mg | B. | 15.2mg | C. | 22.4mg | D. | 60.8mg |