题目内容
15.配制80g溶质质量分数为20%的氯化钠溶液常按以下操作顺序进行.试回答:
(1)B操作中应称量氯化钠的质量是16 g,放好砝码和游码后,向托盘中加入氯化钠时,若指针偏向分度盘的左边,应进行的操作是减少左盘中适量的氯化钠固体.
(2)D操作应选用100 (填“10“或“l00“)mL的量筒.
(3)E中玻璃棒的作用是加速溶解.
分析 (1)根据溶质质量=溶液质量×溶质质量分数进行计算;根据称量一定量固体的操作方法进行回答;
(2)根据量筒的选择方法选择合适的量筒;
(3)根据溶解过程中玻璃棒的作用回答.
解答 解:(1)溶液中溶质的质量=溶液的质量×溶质质量分数,所以需要氯化钠固体的质量=80g×20%=16g;在称量一定量氯化钠时,指针向左偏说明左边的药品多了,所以要减少药品的量至天平平衡;
(2)根据氯化钠固体的质量和溶液的总质量可知需要水的质量为80-16=64g,根据水的密度可知水的体积为64毫升,选择量筒时要依据一次量取,量程最小的原则选取,所以要选择100mL的量筒;
(3)在溶解过程玻璃棒的作用是搅拌加速溶解;
故答案为:(1)16;减少左盘中适量的氯化钠固体 (2)100 (3)加速溶解.
点评 此题属于配制一定溶质质量分数溶液的基础考查,掌握实验原理和实验的注意事项是解答的关键,试题难度不大,注意语言叙述要规范.

练习册系列答案
相关题目
6.(1)今天是化学实验室开放日,老师拿出两瓶无标签的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体,我们对此气体展开了一系列探究:
①此气体是什么物质?验证它的实验方案如下:
产生此气体的化学方程式可能是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②我想制取该气体,采用的发生装置和收集装置可选取如图甲中的BC或BE(填序号).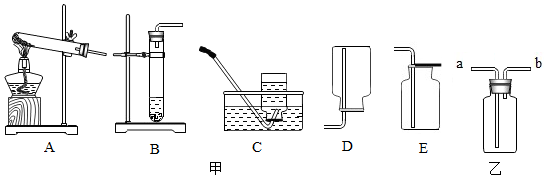
③如图乙装置收集该气体,气体由a端(填“a”或“b”)导入.
(2)某校化学兴趣小组同学在实验室整理药品时,发现氢氧化钠溶液的试剂瓶未塞瓶塞,且试剂瓶口周围有一些白色固体,他们怀疑氢氧化钠已经变质,于是进行了如下实验探究
【提出问题】氢氧化钠是否变质?
【查阅资料】氯化钠溶液、氯化钡溶液呈中性.
【实验探究】小王、小李两同学分别设计了不同方案并加以实验.
(1)小李同学认为小王同学的结论不科学,其理由是变质后生成的碳酸钠溶液显碱性,pH大于7.
(2)小李同学的实验中观察到实验现象A为产生白色沉淀.
(3)小张同学认为该氢氧化钠溶液只是部分变质,于是对小李同学的实验进行如下改进:向试管中加入过量的氯化钡溶液,目的是除去碳酸钠,然后再向溶液中加入酚酞试液,通过观察溶液颜色的变化,说明溶液中含有氢氧化钠.
(4)小王同学在测定溶液pH实验中,由于紧张先将pH试纸润湿后再去测氢氧化钠溶液的pH,你认为他测出该溶液的pH会偏小(填“偏大”“偏小”或“不变”)
①此气体是什么物质?验证它的实验方案如下:
| 猜想与假设 | 实验步骤 | 现象及结论 |
| 此气体可能是氧气 | 收集一瓶该气体,把带火星的木条伸入瓶中. | 带火星的木条复燃,该气体是氧气. |
②我想制取该气体,采用的发生装置和收集装置可选取如图甲中的BC或BE(填序号).

③如图乙装置收集该气体,气体由a端(填“a”或“b”)导入.
(2)某校化学兴趣小组同学在实验室整理药品时,发现氢氧化钠溶液的试剂瓶未塞瓶塞,且试剂瓶口周围有一些白色固体,他们怀疑氢氧化钠已经变质,于是进行了如下实验探究
【提出问题】氢氧化钠是否变质?
【查阅资料】氯化钠溶液、氯化钡溶液呈中性.
【实验探究】小王、小李两同学分别设计了不同方案并加以实验.
| 实验操作 | 实验现象 | 实验结论 | |
| 小王 | 用pH试纸测溶液的pH | 溶液的pH>7 | 说明氢氧化钠溶液没有变质 |
| 小李 | 取少量溶液于试管中,加入适量氯化钡溶液 | A | 说明氢氧化钠溶液已经变质 |
(2)小李同学的实验中观察到实验现象A为产生白色沉淀.
(3)小张同学认为该氢氧化钠溶液只是部分变质,于是对小李同学的实验进行如下改进:向试管中加入过量的氯化钡溶液,目的是除去碳酸钠,然后再向溶液中加入酚酞试液,通过观察溶液颜色的变化,说明溶液中含有氢氧化钠.
(4)小王同学在测定溶液pH实验中,由于紧张先将pH试纸润湿后再去测氢氧化钠溶液的pH,你认为他测出该溶液的pH会偏小(填“偏大”“偏小”或“不变”)
3.如图为元素周期表的一部分.下列叙述错误的是( )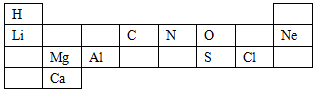

| A. | 钙的核电荷数是20 | |
| B. | 镁在化学反应中较易失去电子 | |
| C. | 每个周期结尾元素的化学性质比较稳定 | |
| D. | 硫离子的符号为是S2+ |
20.实验时有久置的氢氧化钙粉末[Ca(OH)2],化学兴趣小组对该瓶粉末的组成进行实验探究.
(1)提出问题:这瓶氢氧化钙是否已经变质?
(2)假设:该氢氧化钙粉末的成分为①氢氧化钙;②氢氧化钙、碳酸钙;③碳酸钙(写一种).
(3)设计方案、进行实验是否变质:请你参与探究,并填写如表.
(4)思考:氢氧化钙变质是由于Ca(OH)2与空气中的二氧化碳发生化学反应的缘故,因此氢氧化钙应密封 保存.
(1)提出问题:这瓶氢氧化钙是否已经变质?
(2)假设:该氢氧化钙粉末的成分为①氢氧化钙;②氢氧化钙、碳酸钙;③碳酸钙(写一种).
(3)设计方案、进行实验是否变质:请你参与探究,并填写如表.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取样品少量于小烧杯中,加入适量水,充分搅拌,过滤. | ||
| ②滴加足量稀盐酸于滤渣中. | 大量气泡产生 | 氢氧化钙已经变质. |
| (3)取少量滤液于试管中,滴加酚酞试液. | 无色溶液变红色 | 氢氧化钙部分变质. |
7.某同学为了研究化学实验室中某块白色固体的性质,进行了如下实验,你认为其中不正确的实验方案是( )
| A. | 观察固体的颜色和外观 | B. | 放入水中试其溶解性 | ||
| C. | 用嘴尝其味道 | D. | 加热固体观察是否有变化 |