题目内容
20.下列叙述正确的是( )| A. | 长期放置后不会分层的液体一定是溶液 | |
| B. | 在沉淀、吸附、过滤、消毒、蒸馏等净水过程中,消毒净化程度最高 | |
| C. | 稀释浓硫酸时,一定要把浓硫酸沿着器壁慢慢注入水里,并用玻璃棒不断搅拌 | |
| D. | 回收各种白色废弃物品,能有效解决“白色污染”问题 |
分析 A、根据溶液的特点考虑;
B、蒸馏可以得到蒸馏水,属于纯净物;
C、根据浓硫酸的稀释方法考虑;
D、根据废弃塑料是产生“白色污染”的主要原因进行分析.
解答 解:A、长期放置后不会分层的液体不一定是溶液,例如蒸馏水,故A错误;
B、蒸馏可以得到蒸馏水,属于纯净物,所以蒸馏属于净化水程度最高的,故B错误;
C、稀释浓硫酸时,一定要把浓硫酸沿着器壁慢慢注入水里,并不断搅拌,故C正确;
D、废弃塑料是产生“白色污染”的主要原因,白色废弃物品,不是造成“白色污染”原因,故D错误.
故选C.
点评 解答本题关键是知道溶液的特点,熟悉净化水的方法,浓硫酸的稀释方法.

练习册系列答案
相关题目
10.生活中的下列物质中,属于纯净物的是( )
| A. | 白酒 | B. | 碘盐 | C. | 冰水 | D. | 天然气 |
5. 化学小组同学在帮实验员整理药品时,发现一瓶标签残缺的无色溶液(如图1所示),为确定其中溶质的成分,进行了如下探究活动.
化学小组同学在帮实验员整理药品时,发现一瓶标签残缺的无色溶液(如图1所示),为确定其中溶质的成分,进行了如下探究活动.
【做出猜想】
根据标签内容,推测溶质可能为NaOH、NaCl、Na2SO4、NaNO3、Na2CO3、NaHCO3中的一种.
【查阅资料】上述六种物质的相关信息如表:
【分析讨论】小组同学一致认为,溶液中的溶质不可能是NaHCO3,其理由是室温时碳酸氢钠饱和溶液的质量分数小于15%.
【实验探究】小组同学对其余五种猜想继续进行探究.
【反思交流】
小红结合药品的存放环境进行分析,认为溶液中的碳酸钠还有可能是氢氧化钠变质产生的,其变质的化学方程式为2NaOH+CO2═Na2CO3+H2O.因此,溶液中的溶质可能有两种情况:第一种情况是只含Na2CO3;第二种情况是含有氢氧化钠和碳酸钠.
【进一步探究】
为最后确定溶液中溶质的成分,小组同学按如图2所示过程进行实验(已知CaCl2溶液呈中性),步骤③中观察到溶液为红色,因此确认第二种情况成立.
【总结提高】
倾倒液体药品时,为防止标签损坏,应注意标签向着手心,且药品取用完毕后应及时盖好瓶塞.
 化学小组同学在帮实验员整理药品时,发现一瓶标签残缺的无色溶液(如图1所示),为确定其中溶质的成分,进行了如下探究活动.
化学小组同学在帮实验员整理药品时,发现一瓶标签残缺的无色溶液(如图1所示),为确定其中溶质的成分,进行了如下探究活动. 【做出猜想】
根据标签内容,推测溶质可能为NaOH、NaCl、Na2SO4、NaNO3、Na2CO3、NaHCO3中的一种.
【查阅资料】上述六种物质的相关信息如表:
| 物质 | NaOH | NaCl | Na2SO4 | NaNO3 | Na2CO3 | NaHCO3 |
| 常温下的溶解度/g | 109 | 36 | 19.5 | 87 | 21.5 | 9.6 |
| 水溶液的酸碱性 | 碱性 | 中性 | 中性 | 中性 | 碱性 | 碱性 |
【实验探究】小组同学对其余五种猜想继续进行探究.
| 实验操作 | 测定结果或现象 | 得出结论 |
| 取少量待测液于试管中,测溶液的pH | pH>7 | 溶质不可能是氯化钠、硫酸钠、硝酸钠 |
| 取少量待测液于试管中,加入2mL稀盐酸 | 观察到产生气泡 | 溶质是碳酸钠 |
小红结合药品的存放环境进行分析,认为溶液中的碳酸钠还有可能是氢氧化钠变质产生的,其变质的化学方程式为2NaOH+CO2═Na2CO3+H2O.因此,溶液中的溶质可能有两种情况:第一种情况是只含Na2CO3;第二种情况是含有氢氧化钠和碳酸钠.
【进一步探究】
为最后确定溶液中溶质的成分,小组同学按如图2所示过程进行实验(已知CaCl2溶液呈中性),步骤③中观察到溶液为红色,因此确认第二种情况成立.
【总结提高】
倾倒液体药品时,为防止标签损坏,应注意标签向着手心,且药品取用完毕后应及时盖好瓶塞.
9.下列相关事实用粒子的知识解释错误的是( )
| 选项 | 事实 | 解释 |
| A | 蔗糖放到水里会逐渐“消失” | 蔗糖分子很小,并不断运动 |
| B | 金刚石和石墨物理性质差异较大 | 碳原子的排列方式不同 |
| C | 宝石绚丽多彩 | 宝石中含有某些金属原子 |
| D | CO有毒,而CO2无毒 | 分子的结构不同 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
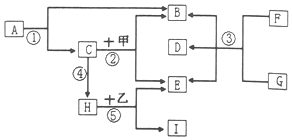 A~I和甲、乙是目前我们已学的常见物质,它们的相互转化如图所示(有的反应条件和反应物未给出).其中A、B的组成元素相同,且常温下都是液体.C是植物光合作用的一种产物,H为一种气体,I是红色固体,③是实验室制取E的反应.
A~I和甲、乙是目前我们已学的常见物质,它们的相互转化如图所示(有的反应条件和反应物未给出).其中A、B的组成元素相同,且常温下都是液体.C是植物光合作用的一种产物,H为一种气体,I是红色固体,③是实验室制取E的反应.