题目内容
14.蛋白质是由多种氨基酸[如:丙氨酸:CH3CH(NH2)COOH等]构成的极为复杂的化合物,人体通过食物获得的蛋白质,在胃肠里与水发生反应,生成氨基酸,试计算:①丙氨酸分子中氮原子与氧原子的个数比1:2,
②丙氨酸的相对分子质量:89,
③丙氨酸中各元素的质量比C:H:N:O=36:7:14:32.
分析 ①根据分子结构来分析解答;
②相对分子质量为构成分子的各原子的相对原子质量之和;
③根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
解答 解:①由化学式可知,每个丙氨酸分子中含有1个氮原子和2个氧原子,所以丙氨酸分子中氮原子与氧原子的个数比1:2;故填:1:2;
②丙氨酸的相对分子质量=12×3+7+16×2+14=89;故填:89;
③丙氨酸分子中C、H、N、O四种元素质量比为(12×3):(1×7):14:(16×2)=36:7:14:32.
故填:C:H:N:O=36:7:14:32.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
4.寻找规律是学习科学的重要方法之一,根据表中某些金属氧化物与稀硫酸发生化学反应的情况,我们也可以发现他们之间的反应规律.
(1)写出氧化铜与稀硫酸反应的化学反应方程式CuO+H2SO4═CuSO4+H2O.
(2)氧化铁与稀硫酸反应生成的硫酸铁中,铁元素的化合价为+3,则硫酸铁的化学式为Fe2(SO4)3.
| 金属氧化物 | 稀硫酸 | 反应方程式 |
| ZnO | H2SO4 | ZnO+H2SO4=ZnSO4+H2O |
| MgO | H2SO4 | MgO+H2SO4=MgSO4+H2O |
| CaO | H2SO4 | CaO+H2SO4=CaSO4+H2O |
| … | … | … |
(2)氧化铁与稀硫酸反应生成的硫酸铁中,铁元素的化合价为+3,则硫酸铁的化学式为Fe2(SO4)3.
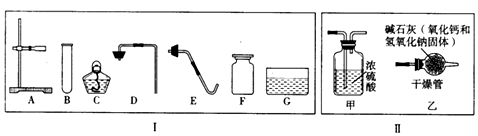
2.如图所示图示中的有关实验操作正确的是( )
| A. |  | B. |  | C. |  | D. |  |
6.除去下列物质中的杂质(括号内物质为杂质)的方法错误的是( )
| A. | CO2(HCl气体)--通过适量的NaOH溶液 | B. | N2(O2)--通过灼热的铜网 | ||
| C. | H2(水蒸气)--通过浓硫酸的洗气瓶 | D. | CO(CO2)--通过灼热的炭层 |
3.下列粒子的化学性质与镁原子  最相似的是( )
最相似的是( )
 最相似的是( )
最相似的是( )| A. |  | B. |  | C. |  | D. |  |
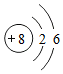 ,它属于原子(填原子或离子),它的原子序数为8,核外电子数为8,属于非金属
,它属于原子(填原子或离子),它的原子序数为8,核外电子数为8,属于非金属