题目内容
10.某兴趣小组对实验室制备氧气的反应条件进行如下探究实验.(1)为探究不同催化剂对氯酸钾分解速度的影响,甲设计以下对比实验探究,在相同温度下,比较两组实验产生O2的快慢.
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g CuO均匀混合加热
实验中Ⅱ中x的值应为3.0g;Ⅰ中反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
实验结论:在其他条件相同的情况下,MnO2的催化能力比CuO强.
(2)乙探究了影响双氧水分解速度的某种因素.实验数据记录和可选装置如表:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |
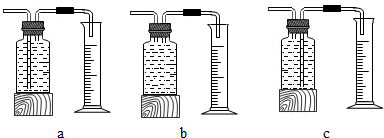
本实验中,测量O2体积的装置应该是C(填编号);
实验结论:乙探究中,在其他条件相同的情况下,双氧水的浓度越大,双氧水分解得越快.
分析 (1)可采用控制变量法,要控制氯酸钾的质量相等才能比较出二氧化锰和氧化铜的催化效果,据此进行分析解答.
(2)测量氧气的体积采用的是排水法,将排出的水的用量筒收集起来,排出的水的体积就是氧气的体积;气体短管进长管出才能排出试剂瓶中的水,据此进行分析解答.
解答 解:(1)控制氯酸钾的质量相等,才能比较出二氧化锰和氧化铜的催化效果,所以Ⅱ中x的数值为3.0g; 氯酸钾在二氧化锰的作用下加热分解产生氯化钾和氧气,反应的方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(2)测量氧气的体积采用的是排水法,将排出的水的用量筒收集起来,排出的水的体积就是氧气的体积;气体短管进长管出才能排出试剂瓶中的水,要将瓶内的水排出来,A和B都不可以,应该选择C装置作为实验装置.
由表格数据分析可知,在相同条件下,双氧水的浓度越大,双氧水分解得越快、
故答案为:(1)3.0; 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3 O2↑;
(2)C;双氧水的浓度越大.
点评 本题难度不大,考查了影响化学反应速率的因素,掌握控制变量法的应用、量气装置等是正确解答本题的关键.

练习册系列答案
相关题目
20.下来有关环境问题的叙述正确的是( )
| A. | 为解决“白色污染”问题,可将废弃塑料焚烧处理 | |
| B. | 汽车使用乙醇汽油可减缓温室效应 | |
| C. | 通过秸秆综合利用,杜绝露天焚烧,来降低空气中PM2.5的含量 | |
| D. | 化工厂通过加高烟囱来排放废弃,以防止形成酸雨 |
19.下列实验方案设计不合理的是( )
| A. | 鉴别铁粉和木炭粉:观察颜色 | |
| B. | 鉴别羊毛和合成纤维:灼烧、闻气味 | |
| C. | 除去铜中混有的氧化铜:加过量稀硫酸,过滤 | |
| D. | 除去氧化钙中混有的碳酸钙:高温煅烧 |
20.现有10克CuO和ZnO的混合物,下列实验方案,不能确定CuO质量分数的是( )
| A. | 将混合物与足量H2充分反应,冷却后测出剩余固体质量 | |
| B. | 将混合物与足量CO充分反应,反应后的气体通入足量的NaOH溶液中,测出NaOH溶液质量的增加值 | |
| C. | 将混合物完全溶于稀H2SO4,加入足量铁粉,充分反应后,过滤、洗涤、干燥,测出剩余固体质量 | |
| D. | 将混合物完全溶于稀H2SO4,加入足量NaOH溶液,过滤、洗涤、干燥,测出剩余固体质量 |

