题目内容
9.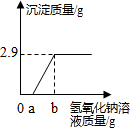 20g氯化镁溶液中混有少量盐酸,往该溶液中滴加足量氢氧化钠溶液,充分反应后得到沉淀的质量与加入氢氧化钠溶液的质量变化关系如图所示.
20g氯化镁溶液中混有少量盐酸,往该溶液中滴加足量氢氧化钠溶液,充分反应后得到沉淀的质量与加入氢氧化钠溶液的质量变化关系如图所示.(1)滴加氢氧化钠溶液的质量≤ag时,反应不产生沉淀,其原因是氢氧化钠不足,由于盐酸的存在氢氧化钠与氯化镁不能生成氢氧化镁沉淀.
(2)求20g氯化镁溶液中氯化镁的质量分数.
分析 向盐酸和氯化镁的混合溶液滴加氢氧化钠溶液,盐酸、氯化镁都可与氢氧化钠发生反应,由于盐酸的存在氢氧化钠与氯化镁不能生成氢氧化镁沉淀,待盐酸反应完才能产生氢氧化镁沉淀;所以图象记录数据中,加入不大于ag氢氧化钠溶液时产生沉淀的质量为0;而在加入氢氧化钠溶液不小于bg时,产生沉淀的质量均为2.9g,说明氯化镁已完全反应,;根据氯化镁与氢氧化钠反应的化学方程式,由沉淀氢氧化镁的质量可计算混合溶液中氯化镁的质量从而可计算出氯化镁的质量分数.
解答 解:
结合图象可知,氢氧化钠的质量≤ag时,反应不产生沉淀,其原因是:氢氧化钠不足,由于盐酸的存在氢氧化钠与氯化镁不能生成氢氧化镁沉淀.
设20g溶液中硫酸镁的质量为x,
MgCl2+2NaOH═Mg(OH)2↓+2NaCl,
95 58
x 2.9g
$\frac{95}{x}=\frac{58}{2.9g}$
x=4.75g
20g氯化镁溶液中氯化镁的质量分数=$\frac{4.75g}{20g}×$10%=23.75%
故答案为:(1)≤a;氢氧化钠不足,由于盐酸的存在氢氧化钠与氯化镁不能生成氢氧化镁沉淀;(2)23.75
点评 学生应熟悉利用化学方程式计算的思路和格式,能利用恰好反应及元素守恒和分析数据来解答.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
20.下列实验操作和分析都正确的是( )
| 操 作 | 分 析 | |
| A | 做铁丝在氧气中燃烧实验时,要预先在集气瓶中放入少量水 | 目的是使燃烧更剧烈 |
| B | 用带火星的木条伸入集气瓶底部来检验CO2是否收集满 | 因为CO2的密度比空气大 |
| C | 做红磷燃烧前后质量的测定实验时,要在密闭容器中进行 | 目的是为了减少环境污染 |
| D | 木炭还原氧化铜时,加热用的酒精灯可加网罩 | 网罩的作用是使火焰集中并提高温度 |
| A. | A | B. | B | C. | C | D. | D |
4.下列实验方案设计不合理的是( )
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 鉴别硝酸铵与氢氧化钠固体 | 水 |
| B | 除去生石灰中少量的碳酸钙 | 加水或盐酸 |
| C | 检验氢氧化钠溶液是否变质 | 稀盐酸或石灰水 |
| D | 除去烧杯内壁沾有的碘 | 酒精洗涤 |
| A. | A | B. | B | C. | C | D. | D |
18.某元素原子核中含有11个质子和12个中子,核外有11个电子,则其相对原子质量( )
| A. | 11 | B. | 23克 | C. | 34 | D. | 23 |
19.二氧化碳通入足量澄清石灰水中,得到的是( )
| A. | 溶液 | B. | 纯净物 | C. | 乳浊液 | D. | 悬浊液 |
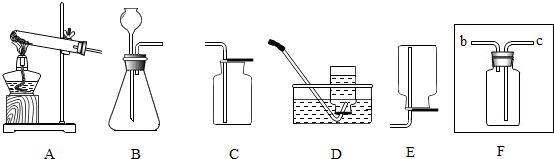
 实验室欲配制5g质量分数为50%的NaCl溶液.试回答下列下列问题.
实验室欲配制5g质量分数为50%的NaCl溶液.试回答下列下列问题.