题目内容
14.硝酸铵是农业生产中的一种常用化肥,请回答:硝酸铵中N、H、O元素的质量比是7:1:12,其中氮元素的质量分数是35%.分析 根据硝酸铵的化学式NH4N03可知,其中氮、氧两种元素的质量比=(氮的相对原子质量×氮原子个数):(氧的相对原子质量×氧原子个数);根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
解答 解:根据硝酸铵的化学式NH4N03可知,硝酸铵中的N、H、O质量比是(14×2):(1×4):(16×3)=7:1:12;
硝酸铵中氮元素的质量分数是$\frac{14×2}{14×2+1×4+16×3}$×100%=35%.
故答案为:
7:1:12;35%.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
19.下列物质的用途中,利用其物理性质的是( )
| A. | 干冰用作制冷剂 | B. | 硫酸用于处理碱性废液 | ||
| C. | 氮气用于食品防腐 | D. | 生石灰用作干燥剂 |
6.下列操作正确的是( )
| A. | 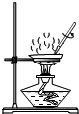 蒸发溶剂 | B. |  稀释浓硫酸 | ||
| C. | 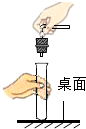 在桌面上塞上橡皮塞 | D. | 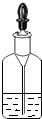 滴瓶上的滴管清洗后放回 |
3.在下列化合物中,元素X的化合价呈现+6价的是( )
| A. | Na2XO3 | B. | XO2 | C. | H2XO3 | D. | H2XO4 |
4.下列物质不属于氮肥的是( )
| A. | NH4NO3 | B. | NH4HCO3 | C. | K2SO4 | D. | CO(NH2)2 |