题目内容
8.通过一段时间的化学学习,应该知道有多种途径可以制取氧气.如:A、电解水B、分离空气C、加热高锰酸钾D、分解过氧化氢 E、加热氯酸钾和二氧化锰的混合物等.
(1)若用如图1装置加热高锰酸钾制取氧气:写出标号仪器的名称 1水槽,2集气瓶;实验结束,停止加热时要先把导管移出水面,其理由是防止水倒流,使试管炸裂,此时发现水槽中的水变成了浅紫红色,你认为产生该现象的原因可能是没有在试管口处塞上一团棉花;
(2)若分解过氧化氢制取氧气,供选用的装置如图2:

要得到平稳的氧气流,应选用的发生装置是甲(选填“甲”或“乙”);若用丙装置收集氧气,气体应从a(选填“a”或“b”)端导入.
分析 (1)熟记仪器的名称以及加热高锰酸钾制取氧气的注意事项来分析;
(2)根据要得到平稳的氧气流,应该选用注射器滴加,氧气密度比空气大进行分析.
解答 解:(1)1是水槽,2是集气瓶;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;在实验前,要在试管口塞上一团棉花,以防高锰酸钾颗粒随氧气流进入水槽而使得水变红色;故填:水槽;集气瓶;防止水倒流,使试管炸裂;没有在试管口处塞上一团棉花;
(2)分解过氧化氢制取氧气,要得到平稳的氧气流,应选用的发生装置是甲,氧气密度比空气大,用丙装置通过排空气法收集氧气,气体应从a端导入.
故填:甲;a.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.在食盐中加入KIO3可防止地方甲状腺肿大,检验食盐中是否含有KIO3,可利用化学反应:5x+KIO3+3H2SO4═3K2SO4+3I2+3H2O,其中x的化学式为( )
| A. | HI | B. | I2O5 | C. | KI | D. | HIO3 |
16.某化学小组为了测定学校附近某矿山石灰石中碳酸钙的质量分数.取样品与足量稀盐酸在烧杯反应(假设样品杂质不与稀盐酸反应也不溶于水.)有关实验数据如表:
(1)根据守恒定律可知,反应生成二氧化碳为4.4g.
(2)求该石灰石样品中碳酸钙的质量分数.(写出计算过程)
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸 | 样品 | 烧杯和其混合物 |
| 150g | 12g | 157.6g | |
(2)求该石灰石样品中碳酸钙的质量分数.(写出计算过程)
3.甲、乙两种物质的溶解度曲线如图所示,下列叙述中,不正确的是( )


| A. | 甲、乙两种物质的溶解度都随温度升高而增大 | |
| B. | t1℃时,甲物质的溶解度等于乙物质的溶解度 | |
| C. | t2℃时,甲、乙饱和溶液中溶质的质量分数相等 | |
| D. | t2℃时,甲物质的溶解度大于乙物质的溶解度 |
13.下列语言叙述中正确的是( )
| A. | 催化剂在化学反应里只是加快化学反应速率 | |
| B. | 化合反应不一定是氧化反应,氧化反应一定是化合反应 | |
| C. | 为了防止“白色污染”,必须禁止使用一切塑料袋 | |
| D. | 给固体物质加热时,试管口要向下倾斜,目的是防止试管炸裂 |
20.下列说法中,正确的是( )
| A. | 污染空气的气体有CO、SO2、CO2 | |
| B. | 水中Ca2+、Mg2+含量过多会造成水体富营养化 | |
| C. | 氢气与空气混合就会发生爆炸 | |
| D. | 氮气的化学性质不活泼,常用作保护气 |
17.某化工厂生产的某固体产品中除了含有在加热条件下不分解,也不与空气成分反应的物质外,还可能含有NaHCO3、Na2CO3中的一种或两种.某化学兴趣小组为探究该固体的成分,称量样品m1g,经充分加热并在干燥的保护气中冷却,至质量不再减轻为止,剩余固体的质量为m2g.下列推断正确的是 ( )
| A. | 若m1=m2,则原样品中无NaHCO3 | |
| B. | 若m1>m2,则原样品中一定有NaHCO3 | |
| C. | 若53m1/84<m2<m1,则原样品中一定有Na2CO3 | |
| D. | 若53m1/84<m2<m1,则原样品中一定无Na2CO3 |
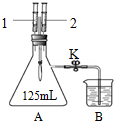 下面是利用如图装置完成验证二氧化碳性质的实验.
下面是利用如图装置完成验证二氧化碳性质的实验.