题目内容
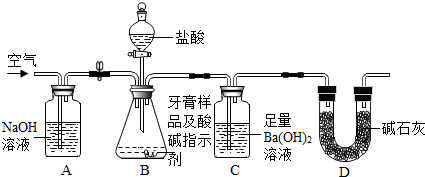
19.某化学兴趣小组在学习了二氧化碳的制法后利用反应原理进行了如图所示实验:(1)该反应的化学方程式为CaC03+2HCl═CaCl2+H20+C02↑;
(2)根据已知条件求解生成的氯化钙的质量(X)的比例式为$\frac{111}{X}$=$\frac{44}{4.4g}$;
(3)该石灰石中碳酸钙的纯度为83.3%(保留一位小数);
(4)用这种石灰石120t制取含杂质的生石灰的质量为76t.

分析 (1)碳酸钙和盐酸反应,生成氯化钙和水和二氧化碳
(2)根据质量守恒定律可知,反应前后减少的质量即为生成的二氧化碳的质量,碳酸钙和盐酸反应,生成氯化钙和水和二氧化碳,根据化学方程式列比例式,可以据此解答;
(3)根据反应的化学方程式结合二氧化碳的质量可求碳酸钙的质量,进而计算该石灰石中碳酸钙的纯度为;
(4)根据碳酸钙煅烧分解生成氧化钙和二氧化碳的化学方程式,可由碳酸钙质量计算出放出二氧化碳的质量,再利用质量守恒定律,石灰石质量减去放出的二氧化碳气体,即得含杂质的生石灰的质量.
解答 解:(1)碳酸钙和盐酸反应,生成氯化钙和水和二氧化碳,化学方程式为CaC03+2HCl═CaCl2+H20+C02↑
(2)根据质量守恒定律可知:生成二氧化碳的质量=100g+12g-107.6g=4.4g
设生成的氯化钙的质量为X,碳酸钙的质量为Y,
CaC03+2HCl═CaCl2+H20+C02↑
100 111 44
Y X 4.4g
$\frac{100}{Y}$=$\frac{44}{4.4g}$
解得:Y=10g
$\frac{111}{X}$=$\frac{44}{4.4g}$
(3)根据(2)的解答可以知道该石灰石中碳酸钙的纯度为$\frac{10g}{12g}$×100%=83.3%.
(4)石灰石120t中碳酸钙的质量为120t×$\frac{10g}{12g}$×100%=100t
设充分煅烧可放出二氧化碳的质量为z
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 44
100t z
$\frac{100}{100t}$=$\frac{44}{z}$
z=44t
可制得含杂质的生石灰的质量=120t-44t=76t
故选D
故答案为:(1)CaC03+2HCl═CaCl2+H20+C02↑
(2)$\frac{111}{X}$=$\frac{44}{4.4g}$
(3)83.3%
(4)76t
点评 根据化学方程式进行计算时,计算所使用的都是纯净物的质量,这在计算时要给以足够的注意.

 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案| A. | 为了增加草莓产量,可以大量使用化肥农药 | |
| B. | 就地焚烧农庄中的秸秆可以增加田地肥效 | |
| C. | 花和草莓的香味不同说明不同分子的性质不同 | |
| D. | 观光电瓶车充电时是化学能转化为电能 |
| 物质 | 醋酸 | 橘子汁 | 草木灰水 | 炉具清洁剂 |
| pH | 2.5 | 3.4 | 11.1 | 12.4 |
| A. | 草木灰水显碱性 | B. | 胃酸过多的人少吃橘子 | ||
| C. | 上述物质酸性最强的是炉具清洁剂 | D. | 醋酸能使紫色石蕊试液变红 |
| A. | NaOH | B. | C6H12O6 | C. | Al2O3 | D. | H2SO4 |
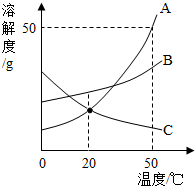
| A. | 50℃时,A物质饱和溶液中溶质的质量分数为50% | |
| B. | 将C的不饱和溶液变为饱和溶液,可采用增加溶质或降低温度的方法 | |
| C. | 将50℃时A、B、C三种物质的饱和溶液降温至20℃,C溶液中溶质质量分数最小 | |
| D. | A中混有少量的B,可用蒸发结晶法提纯 |