题目内容
8.在“观察水的沸腾现象”的实验中,需要加热约150mL的水,要用到的下列仪器是( )①烧杯;②试管;③试管夹;④酒精灯;⑤石棉网;⑥铁架台.
| A. | ①④⑥ | B. | ②③④ | C. | ②③④⑤ | D. | ①④⑤⑥ |
分析 根据烧杯、试管、试管夹、酒精灯、石棉网、铁架台的用途,以及给水加热和量取水的体积的要求判断.
解答 解:观察水的沸腾现象,要有盛水的容器,应在烧杯和试管中选取,但是用水量为150mL,由给试管中的液体加热时,试管中的液体不能超过试管容积的三分之一,则要选择450mL以上的试管,这不可能,所以用烧杯;用烧杯给水加热选择支持固定仪器,要用铁架台;由于烧杯底面积大,易受热不均而炸裂,所以还要用石棉网;酒精灯是热源仪器,加热必须选择酒精灯.
故选:D.
点评 化学是一门以实验为基础的学科,化学实验是考查的重点、难点和热点,特别是基本操作,了解仪器的名称、用途、使用方法和注意事项,是解题的前提.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
18.黄铜(由锌和铜形成的合金)有较强的耐磨性能,在生活中有广泛的用途.三位同学为了测定黄铜屑样品组成,分三次取样品与稀硫酸反应,其实验数据记录如表:
请回答下列问题.
(1)根据质量守恒定律,可算出甲、乙、丙三位同学均生成0.2g氢气,通过对这三位同学的实验数据进行两两对比,可得出丙同学所取的稀硫酸与黄铜最可能符合恰好完全反应;
(2)假如该同学所取的稀硫酸与黄铜恰好完全反应,请求出:
①他所取的黄铜样品中锌的质量分数;
②所得溶液的溶质质量分数.(计算结果精确到0.1%)
| 甲 | 乙 | 丙 | |
| 样品质量/g | 25 | 30 | 25 |
| 稀硫酸质量/g | 120 | 80 | 80 |
| 充分反应后剩余物/g | 144.8 | 109.8 | 104.8 |
(1)根据质量守恒定律,可算出甲、乙、丙三位同学均生成0.2g氢气,通过对这三位同学的实验数据进行两两对比,可得出丙同学所取的稀硫酸与黄铜最可能符合恰好完全反应;
(2)假如该同学所取的稀硫酸与黄铜恰好完全反应,请求出:
①他所取的黄铜样品中锌的质量分数;
②所得溶液的溶质质量分数.(计算结果精确到0.1%)
19.在太空仓中使用新型“氢氧燃料电池”,其化学原理可表示为:2H2+O2$\frac{\underline{\;电池装置\;}}{\;}$2H2O,有关说法错误的是( )
| A. | 该反应是化合反应 | B. | 该电池装置把化学能转化为电能 | ||
| C. | 该电池产生的水可供宇航员使用 | D. | 该反应说明水是由氢气和氧气组成 |
20.小明在做“盐酸中和氢氧化钠溶液”的实验时,滴入盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他对所得溶液的酸碱性进行探究.
探究目的:探究所得溶液的酸碱性
写出该反应的化学方程式:NaOH+HCl=NaCl+H2O.
提出猜想:所得溶液可能呈碱性,也可能呈酸性,还可能呈中性.
实验验证:
分析思考:
(1)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小明提出了以下方案:
方案一:取样,加入金属锌,若观察到冒气泡,则所取溶液呈酸性,若鹜明显现象,则呈中性.
方案二:取样,加入碳酸钠溶液,若有气泡产生,则所取溶液呈酸性,该反应的化学方程式为Na2CO3+2HCl=2NaCl+CO2↑+H2O;若鹜明显现象,则呈中性.
(2)要探究所得溶液的酸碱性,还可用pH试纸进行检测.
探究目的:探究所得溶液的酸碱性
写出该反应的化学方程式:NaOH+HCl=NaCl+H2O.
提出猜想:所得溶液可能呈碱性,也可能呈酸性,还可能呈中性.
实验验证:
| 实验操作 | 实验现象 | 结论 |
| 用试管取该溶液1-2mL,滴入1-2滴无 色酚酞试液,振荡 | 无色酚酞试液变红 | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈中性或酸性 |
(1)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小明提出了以下方案:
方案一:取样,加入金属锌,若观察到冒气泡,则所取溶液呈酸性,若鹜明显现象,则呈中性.
方案二:取样,加入碳酸钠溶液,若有气泡产生,则所取溶液呈酸性,该反应的化学方程式为Na2CO3+2HCl=2NaCl+CO2↑+H2O;若鹜明显现象,则呈中性.
(2)要探究所得溶液的酸碱性,还可用pH试纸进行检测.
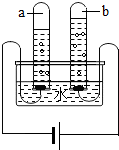 如图所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b.请回答:
如图所示的是电解水实验装置.通电一段时间后,在两个试管中分别收集到气体a和气体b.请回答: