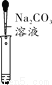��Ŀ����
����̼�����ɫ���С���ѧУ����ͬѧ�������г����У���ش���������

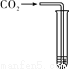
(1)ͼ������ʾ�ĸ������У����ڽ������ϵ���_____(���)
(2)���г�����һ�����������죬ijЩ����Ϊ����֡���ҵ�ϳ��Գ�����(��Ҫ�ɷ�ΪFe2O3)Ϊԭ����������д��һ����̼���������ڸ����·�Ӧ�Ļ�ѧ����ʽ��_____________________________
(3)���ܱ�����������ۣ����ҿ���Ч��ֹ����_______________________�Ӵ������⣮��ֹ�������г������������Ч��ʩ��______________��
(4)���г���Ȧһ�������Ͻ����죬������Ϊ���Ͻ����������ã�����Ʒ�Ƚ���ʴ��ԭ����______
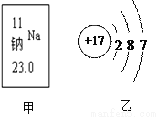
(5)����̫�ȣ�����ͬѧ�dz�̥��ѹ����̫�ߣ����÷��ӡ�ԭ�ӵ����֪ʶ����_______________����Щͬѧ����̼�����ϣ��������ж�����̼���壬������ˮƿ��ʱ����ˮ���Զ��������ԭ����____________���е�ͬѧ�Ǵ��ˡ�ҡҡ�����Ĺ�װ���ϣ������Ϲļв��зֱ�װ��һ�ֹ������ʺ�ˮ������ǰҡ��ʹ���ǻ�ϣ����������¶Ⱦͻή�ͣ����ֹ������ʿ�����_____(����ĸ)
A����ʯ�� B���ռ� C��ʳ�� D�������
(6)Ϊ��ֹ��;��Ƥ����������˸�Ⱦ�������е�ƣ�����е��ܼ���_____(д��ѧʽ)��
(7)ͬѧ�������������ദ�����������ڲ��ɻ�����������_____(����ĸ)��
A����ֽ B����Ƥ C�� ���Ϲ� D���������ϣ�
�ڢ� 3CO+Fe2O32Fe+3CO2 ����������������ˮ Ϳ�� ����������е�������Ӧ�ڱ�������һ�����ܵ�����Ĥ�������ڲ�������ʴ �����������ͣ����Ӽ����� ����ˮƿ�ǣ�ѹǿ��С��������̼���ܽ�ȼ�С���д������ݴ�ƿ���ݳ� D C2H5OH����C2H6O�� B �����������⿼���˳������ϵ�ʶ������ұ����ԭ����������ʴ����������������ܽ�ʱ�����ı仯�������ܽ�ȵ�Ӱ�����أ���������...�������Ϻ�ˮ�����������������Ź㷺Ӧ�á�
�� ˮ�Ǻܺõ��ܼ����±��� NaCl �� KNO3 �ڲ�ͬ�¶�ʱ���ܽ�ȣ��ش����⡣
�¶�/�� | 10 | 20 | 30 | 40 | 50 | 60 | |
�ܽ�� | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
��g/100g ˮ�� | KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 |
I�����������У��ܽ�����¶�Ӱ��仯�ϴ����______��
II��60��ʱ����ͼʾ����

A ����Һ��_______������͡������͡�����Һ��C ����Һ����������_______g��
III��50��ʱ�����������ʵı�����Һ�� 100 g���ֱ�������� 10 g ˮ���ٻָ��� 50�棬 ������˵����ȷ����______��ѡ���ţ���
a���� NaCl ������������ KNO3 ��������
b������Һ���������ܼ��������ȶ�����
c��ʣ����Һ��������NaCl ��Һ���� KNO3 ��Һ d������ NaCl ���� 3.7 g
�� ����Ʒ�ڳ�ʪ�������������⣬��д����ҵ�ϳ�����ķ���_________���û�ѧ����ʽ��ʾ����
�� ijͬѧ��һ�������� Zn �۷��� AgNO3 �� Cu(NO3)2 �Ļ����Һ�У�ʵ��������ͼ��ʾ��
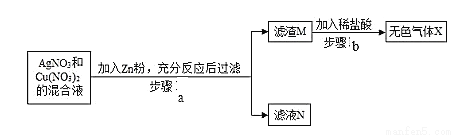
I������ b �����ɵ���ɫ���� X ��_________����Һ N �е�������_____��
II������ a �з�����Ӧ�Ļ�ѧ����ʽ____����дһ�����ɣ���
KNO3 ������ 167.6 cd Fe2O3+6HCl=2FeCl3+3H2O H2 Zn(NO3)2 Zn+2AgNO3=2Ag+Zn(NO3)2�� Zn+Cu(NO3)2=Cu+Zn(NO3)2 ���������� I�����������ܽ�ȱ���֪�������������ܽ�����¶�Ӱ��仯�ϴ����KNO3�� II��60��ʱ��KNO3���ܽ����110.0g����60��ʱ��100gˮ���ܽ�110.0g KNO3...ij��ѧ����Χ�ơ�����кͷ�Ӧ������ѧ���ֳ�����С�鿪չ̽��������������һ���������ʵ��̽����
����ʾʵ�顿��һ����ϡ������뵽ʢ������������Һ��С�ձ��С��÷�Ӧ�Ļ�ѧ����ʽ��____________________________��
���������ϡ�CaCl2��Һ������
��������⡿ʵ����δ�۲쵽����������ͬѧ���������ʣ���Ӧ����Һ�����ʵijɷ���ʲô��
����������衿������ʣ�����ͬѧ�������£�
�����ֻ��CaCl2
�������________
�������CaCl2��Ca(OH)2
���������CaCl2��HCl��Ca(OH)2
����ͬѧ�����ϲ���������ɣ���Ϊ���������������������__________________________��
��ʵ��̽����Ϊ����֤������룬��С���������������������̽����
ʵ�鷽�� | �μ���ɫ ʯ����Һ | ͨ��CO2 | �μ� Na2CO3��Һ |
ʵ����� |
|
|
|
ʵ������ | ________ | ________ | ������ɫ���� |
ʵ����� | ��Һ�к���Ca(OH)2 | ��Һ�к���Ca(OH)2 | ��Һ�к���Ca(OH)2 |
���ó����ۡ�ͨ��̽����ȫ��ͬѧһ��ȷ�����������ȷ�ġ�
�����۷�˼��(1)����ͬѧ��Ϊ�μ�Na2CO3��Һ����������������֤����Һ��һ������Ca(OH)2�������������˵��ԭ��__________________________________��
(2)�ڷ�����Ӧ��������Һ�����ʵijɷ�ʱ�����˿����������⣬����Ҫ����_______________________________________________��
2HCl��Ca(OH)2===CaCl2��2H2O HCl��CaCl2 HCl��Ca(OH)2�ܷ�Ӧ�����ܹ��� ��Һ����ɫ ��Һ����� ��Һ�е��Ȼ���Ҳ�ܺ�̼���Ʒ�Ӧ����̼��ư�ɫ���� ��Ӧ���Ƿ���ʣ�� ������������ʾʵ�顿��һ����ϡ������뵽ʢ����������Һ��С�ձ��С��÷�Ӧ�Ļ�ѧ����ʽ��2HCl+Ca(OH)2=CaCl2+2H2O������������衿���ݷ�Ӧ�����Ķ��ٽ��в���ΪCaCl2��H...��һ���ܱ���������ABCD�������ʣ�������Ӧһ��ʱ���÷�Ӧǰ������ʵ��������±���ʾ
���� | �� | �� | �� | �� |
��Ӧǰ����/g | 34 | 2 | 5 | 5 |
��Ӧ������/g | 0 | x | 5 | 21 |
����˵����ȷ���ǣ� ��
A. �÷�Ӧ�ǻ��Ϸ�Ӧ B. x��ֵΪ18 C. �÷�Ӧ�ǷֽⷴӦ D. ��һ���Ǵ���
C ����������������ѧ��Ӧ���������ӵ�Ϊ������������ٵ�Ϊ��Ӧ���������Ϣ��֪������������34g���Ƿ�Ӧ�������������16g����������������غ㶨�ɿ�֪��Ӧǰ�����ʵ����������䣬������Ӧ����18g���������A. �÷�Ӧ�Ǽס���+��������һ�����������������ʵķֽⷴӦ��ѡ����� B. x��ֵΪ18g+2g=20g��ѡ����� C. �÷�Ӧ�ǷֽⷴӦ ��ѡ����ȷ�� D.������������...