题目内容
20.写出下列反应的符号表达式,并注明反应类型(填“化合反应”或“分解反应”)(1)铁丝在氧气中燃烧:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 反应类型 (化合反应)
(2)镁带燃烧:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO 反应类型(化合反应)
(3)电解水:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ 反应类型 (分解反应)
(4)将二氧化碳通入澄清石灰水中Ca(OH)2+CO2═CaCO3↓+H2O.
分析 根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式.
解答 解:铁在氧气中燃烧生成四氧化三铁,反应的化学方程式为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,属于化合反应;
镁燃烧生成氧化镁,反应的化学方程式为:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO,属于化合反应;
电解水生成氢气和氧气,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,属于分解反应;
二氧化碳能和石灰水中的氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故填:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,化合反应;2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO,化合反应; 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,分解反应;Ca(OH)2+CO2═CaCO3↓+H2O.
点评 书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.“校园有毒塑胶跑道”的风波最近在全国多地出现,劣质的塑胶有一股浓浓的塑胶味扑鼻而来,主要含是甲苯、二甲苯等物质超标,甲苯的化学式为C7H8.下列关于甲苯的说法中正确的是( )
| A. | 甲苯分子的相对分子质量为92 g | |
| B. | 甲苯中含C和H2 | |
| C. | 甲苯由7个碳元素、8个氢元素组成 | |
| D. | 等质量的甲苯和水所含的分子数目比为9:46 |
5.利用下图装置进行实验.实验前K1、K2、K3均已关闭.
【查阅资料】①锌与硫酸反应生成可溶性的硫酸锌和氢气;
②二氧化碳和氢氧化钠反应生成可溶性的碳酸钠和水.
(1)检查装置气密性:保持K1关闭,打开K2、K3,向B中加水至液面浸没下端导管口,用手捂住A瓶外壁,说明装置的左侧气密性良好的现象是B装置左侧导管口有气泡冒出;用同样原理可以检查装置另一侧的气密性.
(2)实验1中,锌与稀硫酸反应的化学方程式是Zn+H2SO4═ZnSO4+H2↑;气体收集完毕后,在不拆卸装置的情况下,使A中未反应的稀硫酸大部分转移到B中的操作是打开k2,k3,关闭k1.
(3)实验2中,二氧化碳与氢氧化钠溶液反应的化学方程式是CO2+2NaOH═Na2CO3+H2O;实验过程中,观察到的现象是B中的水进入A中,约占瓶体积的$\frac{1}{2}$;.
【查阅资料】①锌与硫酸反应生成可溶性的硫酸锌和氢气;
②二氧化碳和氢氧化钠反应生成可溶性的碳酸钠和水.
| 装置 内容 | 【实验1】制备气体 | 【实验2】测定气体含量 |
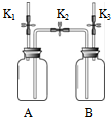 | Ⅰ.打开K1,用注射器向盛有锌粒的A中注入稀硫酸,直至液面浸没下端导管口 Ⅱ.在K1上方导管口收集气体 | Ⅰ.A(容积350mL)中为N2和CO2的混合气,其中CO2的体积分数为50%,B为带刻度的集气瓶且装满水.打开K1,用注射器向A中注入15mL NaOH溶液(足量),关闭K1,充分反应. Ⅱ.打开K2和K3 |
(2)实验1中,锌与稀硫酸反应的化学方程式是Zn+H2SO4═ZnSO4+H2↑;气体收集完毕后,在不拆卸装置的情况下,使A中未反应的稀硫酸大部分转移到B中的操作是打开k2,k3,关闭k1.
(3)实验2中,二氧化碳与氢氧化钠溶液反应的化学方程式是CO2+2NaOH═Na2CO3+H2O;实验过程中,观察到的现象是B中的水进入A中,约占瓶体积的$\frac{1}{2}$;.
10.下列实验操作不正确的是( )
| A. | 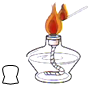 点燃酒精灯 | B. |  添加酒精 | ||
| C. |  存放酒精灯 | D. |  加热碱式碳酸铜 |
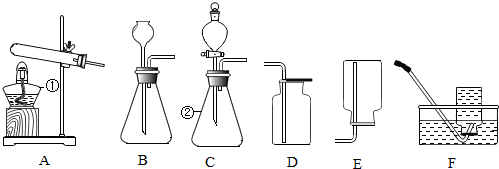
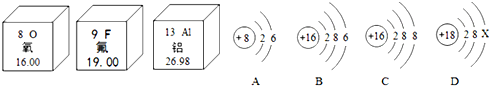
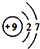 ,氟原子在化学反应中易得到(填“得到”或
,氟原子在化学反应中易得到(填“得到”或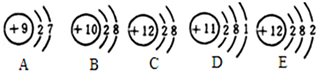
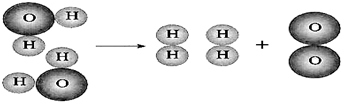
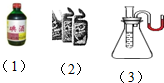 根据下列图片及文字回答问题:
根据下列图片及文字回答问题: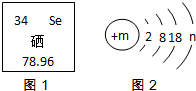 用化学用语表示:
用化学用语表示: