题目内容
加热33.2g氯酸钾和二氧化锰的混合物制氧气,完全反应后剩余23.6g固体物质,求原混合物中氧元素的质量分数.(计算结果保留至1%)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:氯酸钾在二氧化锰催化下受热分解生成氯化钾和氧气,反应中二氧化锰为催化剂其质量在变化前后质量不变;由于反应产生气体氧气,根据质量守恒定律,完全反应前后固体物质的质量差即为放出氧气的质量;
利用反应得到氧气的质量,根据反应的化学方程式,可计算参加反应氯酸钾质量或生成氯化钾质量,由反应前后固体质量与所计算氯酸钾或氯化钾质量差,可得混合物中二氧化锰的质量.进而求出原混合物中氧元素的质量分数.
利用反应得到氧气的质量,根据反应的化学方程式,可计算参加反应氯酸钾质量或生成氯化钾质量,由反应前后固体质量与所计算氯酸钾或氯化钾质量差,可得混合物中二氧化锰的质量.进而求出原混合物中氧元素的质量分数.
解答:解法一:解:由题意可知反应产生的O2质量为33.2g-23.6g=9.6g;
设原混合物中氯酸钾的质量为x.
2KClO3
2KCl+3O2↑
245 96
x 9.6g
=
x=24.5g
原混合物中二氧化锰的质量为33.2g-24.5g=8.7g
原混合物中氧元素质量分数=
×100%=39%
答:原混合物中氧元素质量分数为39%.
解法二:解:由题意可知反应产生的O2质量为33.2g-23.6g=9.6g
设原混合物中氯化钾的质量为y.
2KClO3
2KCl+3O2↑
149 96
y 9.6g
=
y=14.9g
原混合物中二氧化锰的质量为23.6g-14.9g=8.7g
原混合物中氧元素质量为9.6g+8.7g×
×100%=12.8g
原混合物中氧元素质量分数=
×100%=39%
答:原混合物中氧元素质量分数为39%.
设原混合物中氯酸钾的质量为x.
2KClO3
| ||
| △ |
245 96
x 9.6g
| 245 |
| x |
| 96 |
| 9.6g |
x=24.5g
原混合物中二氧化锰的质量为33.2g-24.5g=8.7g
原混合物中氧元素质量分数=
9.6g+8.7g×
| ||
| 33.2g |
答:原混合物中氧元素质量分数为39%.
解法二:解:由题意可知反应产生的O2质量为33.2g-23.6g=9.6g
设原混合物中氯化钾的质量为y.
2KClO3
| ||
| △ |
149 96
y 9.6g
| 149 |
| y |
| 96 |
| 9.6g |
y=14.9g
原混合物中二氧化锰的质量为23.6g-14.9g=8.7g
原混合物中氧元素质量为9.6g+8.7g×
| 32 |
| 87 |
原混合物中氧元素质量分数=
| 12.8g |
| 33.2g |
答:原混合物中氧元素质量分数为39%.
点评:根据质量守恒定律,由反应前后固体物质质量差即反应所产生氧气的质量;利用二氧化锰为反应的催化剂,反应前后质量不变,由混合物质量与参加反应的氯酸钾质量差可求得二氧化锰的质量,进而求出原混合物中氧元素的质量分数.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
温度不变时,向烧杯中加入一定量水,仅有部分晶体溶解.下列说法正确的是( )
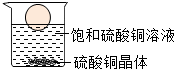

| A、溶液质量增加,溶液蓝色不变 |
| B、物质溶解度不变,塑料球下沉 |
| C、溶质质量增加,溶液浓度变大 |
| D、溶剂质量增加,变为不饱和溶液 |
按一定标准对物质进行分类,给化学学习与研究带来很大的方便.下列各组物质中,符合“氧化物、酸、碱、盐”顺序排列的是( )
| A、HClO、HCl、Mg(OH)2、MgCl2 |
| B、CO2、H2CO3、CaCO3、Ca(HCO3)2 |
| C、H2O、HNO3、NH3?H2O、NH4NO3 |
| D、SO3、NaHSO4、NaOH、Na2SO4 |
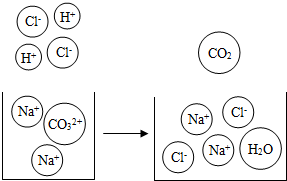 含碳物质在自然界种类繁多,性质各异.
含碳物质在自然界种类繁多,性质各异. 多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界.
多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界.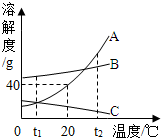 如图为A.B.C.三种物质的溶解度曲线.
如图为A.B.C.三种物质的溶解度曲线.