题目内容
5.某硫酸钠样品中含有少量的碳酸钠,为了测定该样品中硫酸钠的含量,某同学称取35.96克该样品,溶于一定量的水完全溶解得到200克溶液;再加入200克稀硫酸充分搅拌到恰好完全反应(不再放出气泡)为止,称得反应后溶液质量为395.6克.请计算:(1)反应产生的CO2的质量为4.4克;
(2)原混合物中硫酸钠的质量为多少克;
(3)反应后溶液的溶质质量分数?
分析 碳酸钠与稀硫酸反应生成硫酸钠、水和二氧化碳,根据质量守恒定律,混合溶液减少的质量即为生成的二氧化碳质量,据此根据反应的化学方程式列式计算出参加反应碳酸钠的质量、生成硫酸钠的质量,进而计算出原混合物中硫酸钠的质量、反应后溶液的溶质质量分数.
解答 解:(1)反应产生的CO2的质量为200g+200g-395.6=4.4g.
(2)设参加反应碳酸钠的质量为x,生成硫酸钠的质量为y,
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 142 44
x y 4.4g
$\frac{106}{44}=\frac{x}{4.4g}$ x=10.6g
原混合物中硫酸钠的质量为35.96g-10.6g=25.36g.
(3)$\frac{142}{44}=\frac{y}{4.4g}$ y=14.2g
反应后溶液的溶质质量分数为$\frac{25.36g+14.2g}{200g+200g-4.4g}$×100%=10%.
答:(1)4.4;(2)原混合物中硫酸钠的质量为25.36g;(3)反应后溶液的溶质质量分数为10%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出二氧化碳的质量是正确解答本题的前提和关键.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目
16. 2016年1月6日,朝鲜进行氢弹试验,并宣布获得成功,引起国际社会的关注.制氢弹材料需要氢和锂元素;如图是锂元素的部分信息,下列说法错误的是( )
2016年1月6日,朝鲜进行氢弹试验,并宣布获得成功,引起国际社会的关注.制氢弹材料需要氢和锂元素;如图是锂元素的部分信息,下列说法错误的是( )
 2016年1月6日,朝鲜进行氢弹试验,并宣布获得成功,引起国际社会的关注.制氢弹材料需要氢和锂元素;如图是锂元素的部分信息,下列说法错误的是( )
2016年1月6日,朝鲜进行氢弹试验,并宣布获得成功,引起国际社会的关注.制氢弹材料需要氢和锂元素;如图是锂元素的部分信息,下列说法错误的是( )| A. | 锂和钠单质的化学性质相似 | |
| B. | 锂元素为金属元素 | |
| C. | 氢氧化锂硫酸反应的方程式为:Li(OH)2+H2SO4═LiSO4+2H2O | |
| D. | 锂元素的相对原子质量为6.941 |
20.如图为元素周期表第4周期的一部分.据此判断下列说法中错误的是( )
| 26 Fe 铁 55.85 | 27 Co 钴 58.93 | 28 Ni 镍 58.69 | 29 Cu 铜 63.55 |
| A. | 镍元素的符号为N i | |
| B. | 钴元素的相对原子质量是58.93g | |
| C. | 各元素都属于金属元素 | |
| D. | 从左到右各元素的原子序数依次增大 |
10.小明某天早餐所摄入的主要食物有:①面包②牛奶③苹果④鸡蛋⑤黄油.其中富含蛋白质的是( )
| A. | ①② | B. | ②⑤ | C. | ②④ | D. | ①③ |
17.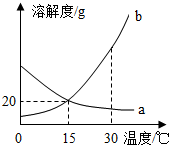 a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是( )
a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是( )
 a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是( )
a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是( )| A. | 15℃时,a、b 的溶解度均为20g | |
| B. | 加水或升温均可使b的饱和溶液变为不饱和溶液 | |
| C. | 将 30℃时a的饱和溶液降温至 15℃,溶质的质量分数不变 | |
| D. | 分别向100g 水中加入 20ga和b,升温至 30℃,所得溶液均为饱和溶液 |
13.下列概念中,前者一定包括后者的是( )
| A. | 化合反应 氧化反应 | B. | 氧化反应 缓慢氧化 | ||
| C. | 混合物 纯净物 | D. | 物理性质 化学性质 |
 由于不良的学习习惯,上网游戏、偏食等因素的影响,青少年患近视的人数不断增加,请利用所学知识,完成以下与近视相关的部分探究活动:
由于不良的学习习惯,上网游戏、偏食等因素的影响,青少年患近视的人数不断增加,请利用所学知识,完成以下与近视相关的部分探究活动: