题目内容
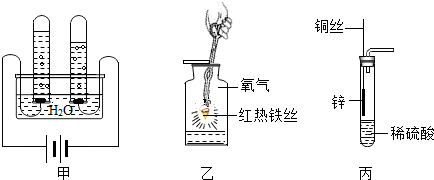
20.为探究铝、铜和锰的金属活动性顺序,某化学兴趣小组进行了如下实验:将大小厚薄相等的三种金属片分别放人盛有同浓度同体积稀硫酸的试管中观察到如下现象:铝和锰表面都有气泡产生,但铝便面产生气泡比锰表面剧烈,而铜表面无明显反应.由此小组成员的出结论:铜的金属活动性顺序排在H后(填“前”或“后”),三种金属的活动性顺序由强到弱的顺序铝>锰>铜.分析 根据金属与酸反应产生气泡的速率可以判断金属的活动性强弱,在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.据此分析有关的问题.
解答 解:将大小厚薄相等的三种金属片分别放人盛有同浓度同体积稀硫酸的试管中,铜表面无明显反应.说明铜的金属活动性顺序排在H后;铝和锰表面都有气泡产生,但铝便面产生气泡比锰表面剧烈,说明铝和锰的金属活动性顺序排在H前,并且铝的金属活动性大于锰,所以三种金属的活动性顺序由强到弱的顺序铝>锰>铜.
故答案为:后;铝>锰>铜.
点评 金属活动性顺序的应用主要表现在两个方面:一是只有排在氢前面的金属才能与酸反应,生成氢气和盐(位置越靠前,反应越剧烈),二是金属与盐溶液的反应时,只有排在前面的金属才能将排在它后面的金属从它的盐溶液中置换出来.

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
11.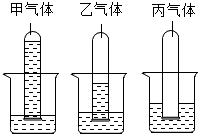 把盛有甲、乙、丙三种气体的试管分别同时倒插入盛有水的烧杯中,一段时间后,观察到如图所示的现象,对甲、乙、丙气体的分析正确的是( )
把盛有甲、乙、丙三种气体的试管分别同时倒插入盛有水的烧杯中,一段时间后,观察到如图所示的现象,对甲、乙、丙气体的分析正确的是( )
 把盛有甲、乙、丙三种气体的试管分别同时倒插入盛有水的烧杯中,一段时间后,观察到如图所示的现象,对甲、乙、丙气体的分析正确的是( )
把盛有甲、乙、丙三种气体的试管分别同时倒插入盛有水的烧杯中,一段时间后,观察到如图所示的现象,对甲、乙、丙气体的分析正确的是( )| A. | 甲、乙、丙气体都易溶于水 | B. | 乙气体比甲气体更易溶于水 | ||
| C. | 不可以用排空气法收集甲气体 | D. | 可以采用排水集气法收集丙气体 |
15.“神舟七号”载人航天飞船常用的液体火箭推进剂主要是偏二甲肼(用R表示),其燃烧的化学方程式为:R+2N2O4═3N2+4H2O+2CO2.则偏二甲肼的化学式是( )
| A. | CH4 | B. | N2H4 | C. | C2H8N2 | D. | C6H7N |
5.家庭厨房里发生的下列变化中,属于物理变化的是( )
| A. | 面包发霉 | B. | 榨取果汁 | C. | 油脂变质 | D. | 菜刀生锈 |
12.下列有关氧气的检验、制备和用途能达到目的是( )
| A. | 氧气具有助燃性 | |
| B. | 氧气可以被点燃 | |
| C. | 过氧化氢分解制取氧气实验中,二氧化锰的量减少 | |
| D. | 将燃着的木条伸入集气瓶,火焰立即熄灭,证明集气瓶中的气体是氧气 |
7. 某化学兴趣小组的同学利用下图实验对碳酸钙高温加热,一段时间,发现石灰水变浑浊,停止加热,同学们对剩余固体的成分进行探究.
某化学兴趣小组的同学利用下图实验对碳酸钙高温加热,一段时间,发现石灰水变浑浊,停止加热,同学们对剩余固体的成分进行探究.
【提出问题】加热后剩余固体的成分是什么?
【提出猜想】
猜想一:碳酸钙全部分解,剩余固体成分为氧化钙,
做出该猜想的依据是(用化学方程式表示)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
猜想二:碳酸钙部分分解,剩余固体成分为氧化钙、碳酸钙.
【方案与结论】
 某化学兴趣小组的同学利用下图实验对碳酸钙高温加热,一段时间,发现石灰水变浑浊,停止加热,同学们对剩余固体的成分进行探究.
某化学兴趣小组的同学利用下图实验对碳酸钙高温加热,一段时间,发现石灰水变浑浊,停止加热,同学们对剩余固体的成分进行探究.【提出问题】加热后剩余固体的成分是什么?
【提出猜想】
猜想一:碳酸钙全部分解,剩余固体成分为氧化钙,
做出该猜想的依据是(用化学方程式表示)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
猜想二:碳酸钙部分分解,剩余固体成分为氧化钙、碳酸钙.
【方案与结论】
| 实验步骤 | 实验现象 | 实验结论 | |
| 步骤1 | 将少量剩余固体放入盛有水的烧杯中,搅拌、静置,滴加少量酚酞 | 烧杯中液体变红 | 猜想二成立 |
| 步骤2 | 向步骤1中的烧杯中滴加盐酸至过量 | 液体由红色变无色,有气泡产生 | |