题目内容
18.如图是实验室制取气体的部分装置.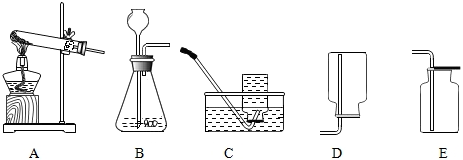
(1)在用上面的两套装置制取气体前,我们首先要检查装置的气密性;
(2)选用A装置加热高锰酸钾制取氧气,该反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)选用B装置制取一瓶干燥的氧气,应选择的收集装置是E(填字母),写出用该方法制取氧气的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
分析 (1)凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
为了防止高锰酸钾进入导管,通常在试管口塞一团棉花;
(3)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
氧气的密度比空气的密度大,不易溶于水.
解答 解:(1)在用上面的两套装置制取气体前,首先要检查装置的气密性.
故填:气密性.
(2)选用A装置加热高锰酸钾制取氧气,该反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)因为氧气的密度比空气大,可以用向上排空气法收集,即用E装置收集,氧气不易溶于水,可以用排水法收集,即用C装置收集,用排水法收集的氧气比用排空气法收集的氧气纯净;
利用B装置制取氧气不需要加热,应该是利用过氧化氢溶液和二氧化锰制取氧气,过氧化氢分解的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
故填:E;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
9.建立宏观与微观的联系是化学学科特有的思维方式.对于下列宏观现象的微观解释中,错误的是( )
| A. | 水通直流电后分解为氢气和氧气,这是因为水分子被破坏,形成了新的分子 | |
| B. | 一氧化碳和二氧化碳具有不同的化学性质,这是因为构成它们的分子不同 | |
| C. | 20mL水与20mL酒精混合后体积小于40mL,是因为混合后分子数目减少 | |
| D. | 俗话说“酒香不怕巷子深”,这一现象说明了分子在永不停息的做无规则运动 |
6.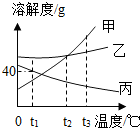 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )| A. | 将相同质量甲、乙的饱和溶液从t3℃降到t2℃,析出甲的质量大 | |
| B. | t3℃时,等质量的甲和乙的饱和溶液中溶质的质量甲>乙 | |
| C. | 分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>丙>甲 | |
| D. | t1℃时,不能配制出溶质的质量分数为40%的丙的饱和溶液 |
13.下列实验中利用提供的方案能达到目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 区分黄铜(Cu,Zn)和黄金 | 加入足量稀盐酸,观察是否产生气泡 |
| B | 鉴别硬水和软水 | 加入少量明矾,搅拌,观察产生泡沫的多少 |
| C | 证明分子间有空隙 | 将1L芝麻和1L大米混合,总体积小于2L |
| D | 检验集气瓶是否集满二氧化碳 | 用带火星的木条放在集气瓶口,木条熄灭 |
| A. | A | B. | B | C. | C | D. | D |
3.去年5月上旬,一枚用于探伤的放射源铱192(其原子中含有77个质子和115个中子)在南京丢失,引起了社会的广泛关注.下列有关说法正确的是( )
| A. | 该元素属于非金属元素 | B. | 该元素的原子序数是192 | ||
| C. | 该原子的核外有77个电子 | D. | 该原子的相对原子质量为192g |
8.下列关于金刚石、石墨、C60的叙述中,不正确的是( )
| A. | 都是由碳元素组成的单质 | |
| B. | 它们的性质完全相同 | |
| C. | 原子的排列方式不同 | |
| D. | 金刚石是自然界最硬的物质,能加工成钻石 |