题目内容
20.13g锌投入到200g硫酸溶液中,恰好完全反应.求:(1)该硫酸溶液的溶质质量分数?
(2)反应后所得溶液的溶质质量分数?
分析 根据锌的质量可以计算稀硫酸中硫酸的质量和生成的硫酸锌的质量,进一步可以计算参加反应的稀硫酸中溶质的质量分数和反应后所得溶液中溶质的质量分数.
解答 解:(1)设稀硫酸中硫酸的质量为x,生成硫酸锌的质量为y,生成氢气的质量为z,
Zn+H2SO4═ZnSO4+H2↑,
65 98 161 2
13g x y z
$\frac{65}{13g}=\frac{98}{x}=\frac{161}{y}=\frac{2}{z}$
x=19.6g
y=32.2g
z=0.4g
参加反应的稀硫酸中溶质的质量分数为$\frac{19.6g}{200g}×$100%=9.8%
反应后所得溶液中溶质的质量分数为:$\frac{32.2g}{13g+200g-0.4g}×$100%≈15.1%
答案:
(1)该硫酸溶液的溶质质量分数为9.8%;
(2)反应后所得溶液中溶质的质量分数为15.1%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
11.某兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的三个实验.

(1)写出A试管中的反应现象粉末逐渐溶解,溶液由无色变成黄色.
(2)写出B试管中发生反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成.同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究.
【提出猜想】
甲同学猜想:NaCl;
乙同学猜想:NaCl、CaCl2;
丙同学猜想:NaCl、CaCl2、HCl;
丁同学猜想:NaCl、Na2CO3.
【查阅资料】NaCl、CaCl2溶液均呈中性.
【交流讨论】甲认为丙同学的猜想一定不正确,理由是产生的白色沉淀是碳酸钙,碳酸钙能和稀盐酸反应,因此碳酸钙和稀盐酸不能共存.
【设计实验】乙、丁两位同学分别设计如下实验验证自己的猜想.
【反思评价】实验结束后,甲认为乙(填“乙”或“丁”)同学的实验结论错误,原因是如果溶液中溶质只有氯化钠,滴加无色酚酞试液时,酚酞试液也不变色.

(1)写出A试管中的反应现象粉末逐渐溶解,溶液由无色变成黄色.
(2)写出B试管中发生反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成.同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究.
【提出猜想】
甲同学猜想:NaCl;
乙同学猜想:NaCl、CaCl2;
丙同学猜想:NaCl、CaCl2、HCl;
丁同学猜想:NaCl、Na2CO3.
【查阅资料】NaCl、CaCl2溶液均呈中性.
【交流讨论】甲认为丙同学的猜想一定不正确,理由是产生的白色沉淀是碳酸钙,碳酸钙能和稀盐酸反应,因此碳酸钙和稀盐酸不能共存.
【设计实验】乙、丁两位同学分别设计如下实验验证自己的猜想.
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 乙 | 取少量滤液于试管中,向取中滴加无色酚酞试液 | 无明显现象 | 猜想正确 |
| 丁 | 取少量滤液于试管中,向其中滴加盐酸 | 产生气泡 | 猜想正确 |
8.在下列反应中,不属于化合反应的是( )
| A. | 硫在氧气中燃烧 | B. | 木炭在空气中燃烧 | ||
| C. | 氯酸钾受热分解 | D. | 镁带在空气中燃烧 |
15.20℃时,向100g未知浓度KCI溶液中加入5g KCl后,正确的是( )
| A. | 溶液质量变为105g | B. | 溶剂质量不变 | ||
| C. | 溶液浓度一定变大 | D. | 溶质质量一定发生变化 |
5.为了保证交通安全,国家颁布实施了更为严厉的酒驾、醉驾处罚措施.酒精监测仪中的反应原理如下化学方程式,则物质X的化学式应为:C2H5OH+4X(红棕色)+6H2SO4═2Cr2(SO4)3(绿色)+2CO2↑+9H2O( )
| A. | CrSO3 | B. | Cr2O3 | C. | Cr2S3 | D. | CrO3 |
9.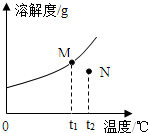 如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
 如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )| A. | 从N→M:先向N中加入适量固体A,再降温至t1℃ | |
| B. | 从N→M:先将N降温至t1℃,再恒温蒸发至有晶体析出 | |
| C. | 从M→N:先将M升温至t2℃,再恒温加入适量水 | |
| D. | 从M→N:先将M升温至t2℃,再恒温将其蒸发掉部分水 |
