题目内容
2.等质量的镁、锌、铁分别与足量的稀硫酸反应,比较产生氢气质量的大小,并画出产生氢气的质量和速率的关系图.分析 根据24份质量的镁和足量的硫酸反应会生成2份质量的氢气,56份质量的铁和足量的稀硫酸反应会生成2份质量的氢气,65份质量的锌和稀硫酸反应会生成2份质量的氢气,所以等质量的镁、锌、铁分别与足量的稀硫酸反应,镁生成的氢气最多,铁次之,锌生成的氢气最少,镁的活动性最强,所以速率最快,其次是锌,反应速率最慢的是铁进行分析.
解答 解:24份质量的镁和足量的硫酸反应会生成2份质量的氢气,56份质量的铁和足量的稀硫酸反应会生成2份质量的氢气,65份质量的锌和稀硫酸反应会生成2份质量的氢气,所以等质量的镁、锌、铁分别与足量的稀硫酸反应,镁生成的氢气最多,铁次之,锌生成的氢气最少,镁的活动性最强,所以速率最快,其次是锌,反应速率最慢的是铁,所以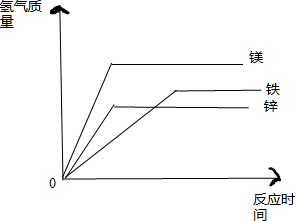
故答案为:
点评 本题主要考查了酸和金属反应的化学方程式的计算,以及金属活动性的应用,难度不大,注意平时加强记忆.

练习册系列答案
相关题目
13.在一定条件下,常温常压下的水可瞬间结成冰,俗称“热冰”,下列说法正确的是( )
| A. | “热冰”是纯净物 | B. | “热冰”在任何条件下都不会融化 | ||
| C. | “热冰”与水的化学性质不同 | D. | 结成“热冰”后,分子停止运动 |
17.下列各物质中加入适量的稀硫酸,不能将杂质除掉的是( )
| A. | 硫酸钠中混有少量碳酸钠 | B. | 氯化钠中混有少量碳酸钠 | ||
| C. | 硫酸钾中混有少量氢氧化钾 | D. | 铜粉中混有少量铁屑 |
