题目内容
12.人体缺钙易产生“骨质疏松症”,补钙保健品“盖中盖”钙片中的有效成分为碳酸钙[CaCO3],试回答:(1)已知钙原子失去最外层2个电子后形成钙离子的结构示意图为
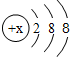 ,则x=20.
,则x=20. (2)列式求碳酸钙的相对分子质量
(3)列式求碳酸钙中钙元素与氧元素的质量比
(4)列式求50克碳酸钙中含钙元素的质量为多少克?
分析 根据碳酸钙的化学式为CaCO3,利用相对原子质量来计算相对分子质量、元素的质量比及元素的质量分数来分析解答.
解答 解:(1)钙离子的质子数-失去电子数=核外电子数,即质子数=核外电子数+失去电子数=2+8+8+2=20;故填:20;
(2)由碳酸钙的化学式为CaCO3,
则其相对分子质量为40+12+16×3=100,
答:碳酸钙的相对分子质量为100;
(3)由碳酸钙的化学式为CaCO3,
则钙、氧两种元素的质量比为40:16×3=5:6,
答:碳酸钙中Ca、O两种元素的质量比为5:6;
(4)由碳酸钙的化学式为CaCO3,
50克碳酸钙中含钙元素的质量为50g×$\frac{40}{100}$×100%=20g,
答:50克碳酸钙中含钙元素的质量为20g.
点评 本题较简单,考查学生利用物质的化学式进行简单计算,明确原子的相对原子质量即可解答.

练习册系列答案
相关题目
2.下列现象用到了氧气的化学性质的是( )
| A. | 用排水法收集氧气 | |
| B. | 氧气能使带火星木条复燃 | |
| C. | 用向上排空气法收集氧气 | |
| D. | 把收集好的氧气用玻璃片盖住正放在桌面上 |
7.为把响水建成高规格文明卫生城市,某同学提出了如下的建议,你认为不正确的措施是( )
| A. | 禁止在城市内燃放烟花爆竹 | |
| B. | 限制燃油车辆的使用,提倡绿色出行 | |
| C. | 街道增设垃圾分类箱 | |
| D. | 提倡使用一次性发泡塑料餐具和塑料袋 |
17.2015年5月31日是第28个“世界无烟日”.吸烟不仅危害自身健康,而且危害他人健康,不吸烟的人易吸到二手烟,从分子的角度解释是( )
| A. | 分子不停地运动 | B. | 分子质量小 | C. | 分子间有间隙 | D. | 分子体积小 |
1.在食盐中加碘可有效预防甲状腺肿大的发生.下图是某地市场销售的一种“加碘食盐”包装袋上的部分说明,请回答问题:
(1)加碘食盐中的“碘”是指D(填字母).
A.碘分子 B.碘原子 C.碘离子 D.碘元素
(2)由储藏方法和食用方法可推测碘酸钾的化学性质之一是受热易分解.
(3)碘酸钾的化学式为KIO3,则碘酸钾中碘元素的化合价为+5;碘酸钾的相对分子质量为214,碘酸钾中K、I、O三种元素的质量比为39:127:48.
(4)根据表中数据计算,每500克该加碘食盐中碘酸钾的质量范围是B(填字母)
A.15~30mg B.25~51mg C.51~101mg
(5)2011年日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,个别居民疯狂抢购食盐.其实防核辐射最有效的方法是服用碘片,假设某人经医生确认,每日需要补充166mg碘化钾(化学式为KI),如果用上述加碘盐来补充等量的碘,则每日至少需食用该加碘食盐的质量是多少千克?(写出计算过程,结果保留一位数字)
| 配料表 | 氯化钠、碘酸钾(KIO3) |
| 含碘量(以I计)/kg | 30mg~60mg |
| 包装日期 | 见封底 |
| 储存方法 | 避热、避光、密封 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
A.碘分子 B.碘原子 C.碘离子 D.碘元素
(2)由储藏方法和食用方法可推测碘酸钾的化学性质之一是受热易分解.
(3)碘酸钾的化学式为KIO3,则碘酸钾中碘元素的化合价为+5;碘酸钾的相对分子质量为214,碘酸钾中K、I、O三种元素的质量比为39:127:48.
(4)根据表中数据计算,每500克该加碘食盐中碘酸钾的质量范围是B(填字母)
A.15~30mg B.25~51mg C.51~101mg
(5)2011年日本强烈地震后,海啸引发福岛第一核电站的放射性物质外泄,个别居民疯狂抢购食盐.其实防核辐射最有效的方法是服用碘片,假设某人经医生确认,每日需要补充166mg碘化钾(化学式为KI),如果用上述加碘盐来补充等量的碘,则每日至少需食用该加碘食盐的质量是多少千克?(写出计算过程,结果保留一位数字)
2.酚酞(C20H14O4)是实验室常用的药品.下列说法不正确的是( )
| A. | 属于氧化物 | B. | 1个分子中含有38个原子 | ||
| C. | 相对分子质量为318 | D. | 由碳、氢、氧三种元素组成 |