题目内容
1.根据质量守恒定律,3g碳在10g氧气中充分燃烧后可以生成二氧化碳11g.分析 根据碳与氧气反应的方程式,由碳与氧气质量比,判断完全反应的物质.再计算出生成的二氧化碳的质量.
解答 解:由C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2可知,碳与氧气的质量比是3:8,则3g碳在10g氧气中充分燃烧,剩余的是氧气.
设3g碳充分燃烧生成的二氧化碳的质量为x
C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2
12 44
3g x
$\frac{12}{3g}=\frac{44}{x}$
解得:x=11g
答案:11g.
点评 本考点考查了质量守恒定律,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,还要条件“恰好完全反应”或“充分反应”等,本考点主要出现在计算题中.

练习册系列答案
相关题目
9.煤气中加人有特殊气味的乙硫醇可提示煤气是否泄漏.乙硫醇(用X表示)燃烧时发生的反应为:2X+9O2 $\frac{\underline{\;点燃\;}}{\;}$4CO2十2SO2十6H2O,则X是( )
| A. | C4H12S2 | B. | C2H6 | C. | C2H6O2 | D. | C2H6S |
16.化学反应的程度与反应物的浓度之间有一定的规律可循.某实验小组各取等质量的木炭和等质量的硫分别在容积相同的机器瓶中燃烧.记录如下:
A、B两组实验属于什么基本反应类型:化合反应.
| 实验 | 实验步骤 | 实验现象 | 燃烧反应的文字表达式 | |
| A | ①木炭在空气中燃烧 | ①木炭红热 | 产生的气体都能使澄清石灰水变浑浊 | 碳+氧$\stackrel{点燃}{→}$二氧化碳 |
| ②木炭在氧气中燃烧 | ②木炭在氧气中燃烧比在空气中燃烧更旺,发出白光,放出更多的热量 | |||
| B | ③硫在空气中燃烧 | ③微弱的淡蓝色火焰 | 产生的气体都有刺激性气味 | 硫+氧气$\stackrel{点燃}{→}$二氧化硫 |
| ④硫在氧气中燃烧 | ④硫在氧气中燃烧发出明亮的蓝紫色火焰,放出更多的热量 | |||
6.下列成语包含化学变化的是( )
| A. | 刻舟求剑 | B. | 火树银花 | C. | 风吹草动 | D. | 量体裁衣 |
13.下列说法错误的是( )
| A. | 营养素就是营养元素的简称 | |
| B. | 使用铁制炊具可以预防缺铁性贫血 | |
| C. | 进食牛奶、豆制品等食物,可以预防儿童佝偻症 | |
| D. | 食用牡蛎等海产品,可以防止因缺锌引起的食欲不振和发育不良 |
11.下列实验操作正确的是( )
| A. |  | B. |  | ||
| C. | 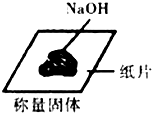 | D. | 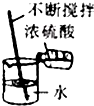 |