题目内容
7.微观角度.用“ ”表示碳原子,“
”表示碳原子,“ ”表示氮原子,“
”表示氮原子,“ ”表示氧原子.
”表示氧原子.(1)用“
 ”表示的物质,固态时俗称为干冰.
”表示的物质,固态时俗称为干冰.(2)同温同压下,气体的体积比等于分子个数比.若空气中其它成分忽略不计,如图可表示空气微观模型的是C.

分析 (1)根据二氧化碳固态时俗称为干冰解答;
(2)根据氧气约占空气体积的$\frac{1}{5}$解答;
解答 解:
(1)用“ ”表示的物质,为二氧化碳,固态时俗称为 干冰;
”表示的物质,为二氧化碳,固态时俗称为 干冰;
(2)同温同压下,气体的体积比等于分子个数比.若空气中其它成分忽略不计,氧气约占空气体积的$\frac{1}{5}$,故图中可表示空气微观模型的是C;
答案:
(1)干冰;(2)C.
点评 本题主要考查了氧气的工业制法、空气组成的测定及对实验数据的分析,比较综合,要细心分析.

练习册系列答案
相关题目
18.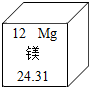 元素周期表中,镁元素的信息如图所示,对图中信息解释不正确的是( )
元素周期表中,镁元素的信息如图所示,对图中信息解释不正确的是( )
 元素周期表中,镁元素的信息如图所示,对图中信息解释不正确的是( )
元素周期表中,镁元素的信息如图所示,对图中信息解释不正确的是( )| A. | 核外电子数为 24 | B. | 原子序数为12 | ||
| C. | 元素符号为Mg | D. | 相对原子质量为24.31 |
15.氢氧化钙常用于改良酸性土壤,其俗称为( )
| A. | 生石灰 | B. | 大理石 | C. | 石灰石 | D. | 熟石灰 |
2.如表实验方法一定能达到实验目的是( )
| 选项 | 实验目的 | 实验方法 |
| A | 除去CO2中的少量CO | 点燃 |
| B | 鉴别石灰水和NaOH溶液 | 加入适量的紫色石蕊溶液 |
| C | 鉴别H2和CH4 | 分别点燃,在火焰上方罩一干冷烧杯 |
| D | 比较Zn、Cu、Ag的金属活动性 | 将Zn和Ag分别放入CuSO4溶液中 |
| A. | A | B. | B | C. | C | D. | D |
12.工业烟气脱硫就是将烟气中含有的二氧化硫除去.采用“双碱法”脱硫的工业流程如图.
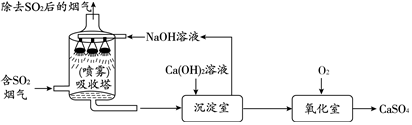
(1)吸收塔中,用NaOH溶液吸收SO2生成亚硫酸钠(Na2SO3)和水,NaOH溶液喷成雾状能充分吸收SO2的原因是增大吸收面积.
(2)沉淀室中发生的是复分解反应,化学方程式为Na2SO3+Ca(OH)2═CaSO3↓+2NaOH.
(3)氧化室中,化学反应的基本类型是化合反应.
(4)已知部分原料的价格如表所示.
上述工业流程中,处理相同量的SO2,双碱法所需的原料成本比用NaOH直接吸收更低,原因是实现了NaOH的循环利用,减少了NaOH的用量.

(1)吸收塔中,用NaOH溶液吸收SO2生成亚硫酸钠(Na2SO3)和水,NaOH溶液喷成雾状能充分吸收SO2的原因是增大吸收面积.
(2)沉淀室中发生的是复分解反应,化学方程式为Na2SO3+Ca(OH)2═CaSO3↓+2NaOH.
(3)氧化室中,化学反应的基本类型是化合反应.
(4)已知部分原料的价格如表所示.
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.90 |
5.用托盘天平称量10.2克(1克以下用游码)药品,如果称后发现误将砝码和称量物的置放颠倒了,则实际称得的药品质量为( )
| A. | 10.2克 | B. | 10克 | C. | 9.8克 | D. | 9克 |
6.在一个密闭容器中有四种物质,在一定条件下充分反应后,测得反应前后各物质的质量如下:
已知X的相对分子质量为n,Q的相对分子质量为2n,则下列推断正确的是( )
| 物 质 | X | Y | Z | Q |
| 反应前质量/g | 4 | 10 | 1 | 21 |
| 反应后质量/g | 0 | 12 | 15 | 待测 |
| A. | 反应后生成14g Z | |
| B. | 反应中Y与Q发生改变的质量比为1:1 | |
| C. | 反应后Q的质量为12g | |
| D. | 该反应方程式中X与Q的化学计量数之比为2:3 |
