题目内容
14.图1是氯化钠和硝酸钾两种物质的溶解度曲线,图2是氢氧化钙的溶解度曲线.根据图示回答下列问题.
(1)10℃时氯化钠的溶解度大于(填“大于”“小于”或“等于”)硝酸钾的溶解度.将30℃时的硝酸钾饱和溶液转变为不饱和溶液的一种方法是升温.从氯化钠溶液中结晶出氯化钠的方法是蒸发溶剂.
(2)某同学从一瓶久置的氢氧化钙固体样品中取出0.2g,加入到30℃时100g水中,充分溶解后过滤,称得剩余固体0.08g.请你判断:滤液为不饱和(填“饱和”或“不饱和”)溶液,剩余固体的成分为碳酸钙.
(3)将20℃时恰好饱和的硝酸钾溶液升温至60℃,一定没有变化的是①②③(填序号).
①水的质量②溶液中溶质的质量③溶质的质量分数④硝酸钾的溶解度.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)观察图表可以看出,10℃时氯化钠的溶解度大于硝酸钾的溶解度;因为硝酸钾的溶解度随温度的上升而增大,要使30℃时的硝酸钾饱和溶液转变为不饱和溶液,可以升高温度或增加溶剂;因氯化钠的溶解度受温度的影响不大,我们可以将溶液加热蒸发,使溶液达到饱和后,在蒸发掉溶剂,溶质就会结晶析出;
(2)从氢氧化钙的溶解度曲线图可以看出,30℃时,氢氧化钙的溶解度是0.15克,而现在100克水中溶解的氢氧化钙的质量是0.2克-0.08克=0.12克,故滤液为不饱和溶液;如果全是氢氧化钙剩余的不溶固体应该是0.05g,剩余固体0.08g所以可以肯定一部分氢氧化钙已经和二氧化碳反应,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,所以久置于空气中的氢氧化钙固体样品中含有碳酸钙;
(3)溶解度受温度的影响较大,升温后,溶解度变大;尽管硝酸钾的溶解度随着温度的升高而增大,但由于升温后溶液的组成可能不变,故溶质的质量、溶剂水的质量、溶液的质量可能不变,故溶液中溶质的质量分数可能不变.
故答案为:(1)大于,升温或加水,蒸发溶剂;
(2)不饱和,碳酸钙或CaCO3;
(3)①②③.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
9.据央视报道,有不法酒类生产企业在白酒中添加酯类物质以增强口感.表中是几种常见的酯.
(1)比较归纳是学习化学的重要方法,上述物质的共同特点有组成元素相同(写出一条即可).
(2)甲酸甲酯(C2H4O2)中碳、氢、氧的原子个数比为1:2:1.
(3)据表推测X的化学式为C4H8O2.
(4)实验测得由甲酸甲酯(C2H4O2)、甲酸乙酯(C3H6O2)组成的混合物中碳元素的质量分数是43.2%,则氧元素的质量分数是49.6%,混合物中甲酸甲酯的质量分数是63%.
| 酯的名称 | 甲酸甲酯 | 甲酸乙酯 | 乙酸甲酯 | 乙酸乙酯 |
| 化学式 | C2H4O2 | C3H6O2 | C3H6O2 | X |
(2)甲酸甲酯(C2H4O2)中碳、氢、氧的原子个数比为1:2:1.
(3)据表推测X的化学式为C4H8O2.
(4)实验测得由甲酸甲酯(C2H4O2)、甲酸乙酯(C3H6O2)组成的混合物中碳元素的质量分数是43.2%,则氧元素的质量分数是49.6%,混合物中甲酸甲酯的质量分数是63%.
19.如图有关实验现象描述不正确的是( )
| A. |  细铁丝在空气中剧烈燃烧 | B. |  蜡烛逐渐熄灭 | ||
| C. |  铝片上有划痕 | D. |  冷却后粗铜丝b端略上升 |
6.如图化学药品保存或实验操作正确的是( )
| A. |  保存浓盐酸 | B. |  保存固体氢氧化钠 | ||
| C. |  稀释浓硫酸 | D. | 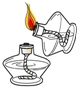 点燃酒精灯 |
3.物质可根据其成份,分为混合物和纯净物,下列物质属于纯净物的是( )
| A. | 氨水 | B. | 盐酸 | C. | 浓硫酸 | D. | 烧碱 |
 碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3).如图是超市销售的一种加碘盐标签上的部分文字说明.
碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3).如图是超市销售的一种加碘盐标签上的部分文字说明.