题目内容
硫酸亚铁晶体 (FeSO4?7H2O)的摩尔质量为 ,
1mol硫酸亚铁晶体分子中含 mol氧原子、 个铁原子.
1mol硫酸亚铁晶体分子中含
考点:有关化学式的计算和推断
专题:化学式的计算
分析:摩尔质量以g/mol作单位,数值上等于其相对分子质量或相对原子质量,据此解答.
根据N=nNA,结合分子构成来计算原子个数.
根据N=nNA,结合分子构成来计算原子个数.
解答:解:FeSO4?7H2O的相对分子质量为:56+32+16×4+7×(2+16)=278,则酸亚铁晶体 (FeSO4?7H2O)的摩尔质量为278g/mol,
n(0)=11n(FeSO4?7H2O)=11×1mol=11mol;
n(Fe)=n(FeSO4?7H2O)=1×1mol=1mol;
N=nNA=1mol×6.02×1023/mol=1.0×1023,
故答案为:278g/mol;11;1.0×1023.
n(0)=11n(FeSO4?7H2O)=11×1mol=11mol;
n(Fe)=n(FeSO4?7H2O)=1×1mol=1mol;
N=nNA=1mol×6.02×1023/mol=1.0×1023,
故答案为:278g/mol;11;1.0×1023.
点评:本题考查了摩尔质量,难度不大,旨在考查学生对基础知识的掌握,加强基础知识的积累.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
下列课题不属于化学学科研究领域的是( )
| A、蛟龙号载人潜水器外壳所需材料的研制 |
| B、我国“神舟”系列飞船需要的高能燃料 |
| C、研究药物对抗“埃博拉”病毒 |
| D、360电脑办公软件的新功能 |
下列物质中存在在氧分子的是( )
| A、二氧化碳 | B、过氧化氢 |
| C、空气 | D、高锰酸钾 |
下列有关物质的用途,所利用的性质与另外三种有根本区别的是( )
| A、用氧气急救病人 |
| B、镁粉用做烟花和照明弹 |
| C、铜丝用做电线 |
| D、用氮气作为瓜果蔬菜的保护气 |
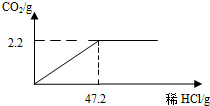 某化学兴趣小组的同学采集了一些大理石样品,为了测定样品中碳酸钙的质量分数,取样品8g粉碎成粉末置于烧杯中,向其中加入一定质量分数的稀盐酸并不断搅拌,反应的关系如图所示:
某化学兴趣小组的同学采集了一些大理石样品,为了测定样品中碳酸钙的质量分数,取样品8g粉碎成粉末置于烧杯中,向其中加入一定质量分数的稀盐酸并不断搅拌,反应的关系如图所示:
